Ung thư biểu mô tế bào vảy xâm lấn sớm của âm hộ là gì?
31 Tháng Một, 2021Contents Tổng quan về ung thư biểu mô tế bào vảy xâm lấn sớm của âm hộ Ung thư...
Tổng quan về bệnh bạch cầu nonlymphocytic cấp tính ở trẻ em
Cấp tính myeloid leukemia (AML) cũng tương tự như người lớn (<50 tuổi) về những thay đổi sinh học phân tử và phản ứng hóa học trị liệu. AML ở trẻ sơ sinh và trẻ nhỏ có nhiều khả năng phát triển bệnh bạch cầu ngoài tủy hơn người lớn.

Contents
1. Căn nguyên của nguyên nhân gây bệnh bạch cầu ở trẻ em vẫn chưa được rõ ràng, các yếu tố nguy cơ có thể xảy ra bao gồm các khía cạnh sau.
(1) Các yếu tố vật lý và hóa học: Mặc dù đã có một số lượng lớn các nghiên cứu về mối tương quan giữa các yếu tố môi trường và tỷ lệ mắc bệnh bạch cầu, các yếu tố liên quan duy nhất được xác định là bức xạ ion hóa. Ví dụ, tiếp xúc với benzen và bức xạ ion hóa có liên quan đến sự khởi phát của AML, nhưng các yếu tố gây bệnh riêng lẻ có thể được xác định rõ ràng chỉ chiếm một phần rất nhỏ tỷ lệ mắc bệnh. Một nghiên cứu về những người sống sót trong khu vực bị ném bom nguyên tử ở Hiroshima và Nagasaki, Nhật Bản cho thấy tỷ lệ mắc bệnh bạch cầu tăng từ 5 đến 15 năm sau vụ nổ, và tỷ lệ mắc AML tăng gấp 20 lần, và đỉnh điểm là 6 đến 8 năm sau khi nhận bức xạ. Nguy cơ mắc bệnh bạch cầu liên quan đến liều lượng bức xạ nhận được. Tuy nhiên, các nghiên cứu tiếp theo về vụ tai nạn hạt nhân ở Đảo Ba Dặm và Chernobyl không tìm thấy bất kỳ mối tương quan nào với bệnh bạch cầu ở trẻ em. Hút thuốc khi mang thai cũng làm tăng tỷ lệ mắc AML. Trong khối u thứ hai , AML là một loại phổ biến hơn, chủ yếu liên quan đến việc tiếp xúc trước đó với các tác nhân alkyl hóa như cyclophosphamide, mù tạt nitơ, busulfan, vv Nó thường xuất hiện từ 4 đến 5 năm sau khối u đầu tiên. Nó được biểu hiện thành hội chứng loạn sản tủy (MDS) và sau đó phát triển thành AML, nhưng tỷ lệ mắc AML giảm sau 10-12 năm. Ngoài ra, việc tiếp xúc với podophyllotoxin VP-16 có liên quan đến sự khởi phát của AML ung thư thứ hai, thường sớm hơn so với những trường hợp gây ra bởi các tác nhân alkyl hóa. Vào những năm 1950, có nhiều thông tin cho rằng chiếu tia X vào tử cung của phụ nữ mang thai sẽ làm tăng nguy cơ mắc bệnh bạch cầu ở trẻ em, tuy nhiên quan điểm này vẫn còn nhiều tranh cãi. Cũng có những nghiên cứu hiện tại cho thấy rằng việc cha mẹ tiếp xúc với bức xạ mức độ thấp trước khi mang thai làm tăng nguy cơ mắc bệnh bạch cầu ở trẻ sơ sinh. Các nghiên cứu đa trung tâm đã chỉ ra rằng việc người mẹ tiếp xúc với thuốc diệt côn trùng, thuốc diệt cỏ và thuốc diệt nấm trước và trong khi mang thai và nghề nghiệp của người cha có liên quan đến sự khởi phát bệnh bạch cầu ở trẻ em.
Mối tương quan giữa điện từ trường và tỷ lệ mắc bệnh bạch cầu đã được báo cáo ngay từ những năm 1970. Tuy nhiên, các nghiên cứu quy mô lớn sau đó đã không xác nhận giả thuyết rằng trường điện từ cường độ thấp có liên quan đến bệnh bạch cầu ở trẻ em và các khối u khác ở trẻ em. Trong những năm gần đây, kết quả nghiên cứu của Hoa Kỳ, Canada và Anh cho rằng tiếp xúc với từ trường cường độ cao (> 0,4μT) có thể làm tăng nguy cơ mắc bệnh bạch cầu cấp tính, trong khi từ trường cường độ thấp ít ảnh hưởng đến cơ thể.
Các nghiên cứu gần đây cũng chỉ ra rằng dung môi hữu cơ gia dụng có liên quan đến sự xuất hiện của bệnh bạch cầu cấp tính ở trẻ em.
Tiếp xúc nghề nghiệp với benzen có liên quan chặt chẽ đến sự xuất hiện của bệnh bạch cầu cấp tính ở người lớn. Mặc dù TẤT CẢ thời thơ ấu không thể do tiếp xúc nghề nghiệp, nhưng nồng độ benzen ngày càng tăng trong môi trường có thể là một trong những nguyên nhân gây ra TẤT CẢ thời thơ ấu. Các nghiên cứu đã báo cáo rằng trẻ em sống trong các trục giao thông hoặc gần trạm xăng (trong vòng 100m) có nguy cơ mắc bệnh bạch cầu cao hơn. Kết quả này dựa trên các nghiên cứu sinh thái học và mối tương quan chính xác cần được xác nhận bởi các nghiên cứu sâu hơn. Kết quả một cuộc nghiên cứu trên hơn 1.000 trẻ em mắc bệnh bạch cầu ở Trung Quốc cho thấy. 46% hộ gia đình đã trang trí nội thất trong vòng 6 tháng trước khi phát hiện bệnh. Cơ chế có thể có của benzen dẫn đến bệnh bạch cầu ở trẻ em có liên quan đến tính nhạy cảm mạnh mẽ của cá nhân ở trẻ em và tính đa hình di truyền của cytochrome p4502E1, myeloperoxidase (MPO), glutathione sulfur transferase (GSTs), v.v. Và những dị tật di truyền vốn có ở trẻ.
(2) Virus: Một loại virus liên quan đến sự khởi phát của AML vẫn chưa được xác nhận.
(3) Yếu tố di truyền: Cho đến nay, sự liên quan của các yếu tố di truyền vẫn chưa được xác nhận ở hầu hết trẻ mắc AML, và thỉnh thoảng có báo cáo về bệnh của anh chị em hoặc gia đình. Trẻ em mắc hội chứng Down có nguy cơ phát triển AML cao gấp 14 lần so với dân số bình thường. Ở những cặp sinh đôi cùng trứng, nếu một đứa trẻ mắc bệnh trước 6 tuổi thì khả năng mắc bệnh của đứa trẻ còn lại là khoảng 20%; đối với những đứa trẻ mắc bệnh trước 1 tuổi thì khả năng mắc bệnh của đứa trẻ còn lại tăng lên rất nhiều; và đứa trẻ đầu tiên là khi 6 tuổi. Trong tương lai, cơ hội phát triển của một đứa trẻ khác sẽ thấp hơn đáng kể so với những đứa trẻ trước 6 tuổi. Cơ hội mắc AML trong một số bệnh lý tủy bẩm sinh cũng tăng lên. Người ta đã chứng minh rằng một số hội chứng di truyền nhất định, chẳng hạn như hội chứng tam nhiễm 21 (hội chứng Down) và bệnh thiếu máu Fanconi , có liên quan mật thiết đến tính nhạy cảm với bệnh bạch cầu. Các nghiên cứu ở Anh và Mỹ cho thấy 2,3% đến 2,6% bệnh bạch cầu cấp tính ở trẻ em có liên quan đến yếu tố di truyền.
Việc điều tra anh chị em, cha mẹ và con đẻ của tất cả các loại bệnh nhân ung thư máu không tìm thấy bất kỳ tỷ lệ mắc khối u cao nào. Mặc dù đã có báo cáo về bệnh bạch cầu ở đồng bào lần lượt, tỷ lệ mắc bệnh cực kỳ thấp. Những cặp song sinh giống hệt nhau có nhiều khả năng mắc bệnh bạch cầu hơn những cặp song sinh cùng cha khác mẹ. Những người bị dị tật di truyền giữa ông bà, cha mẹ và đồng hương có liên quan đến sự khởi phát của nhiều loại TẤT CẢ, bao gồm các bệnh cơ xương khớp, bệnh đường tiêu hóa, bệnh dị ứng, bệnh tim di truyền và bệnh phổi .
Vì đã có đủ số trường hợp sống lâu trong những năm gần đây, một số học giả đã nghiên cứu nguy cơ mắc bệnh bạch cầu ở con của những bệnh nhân sống lâu và không tìm thấy sự gia tăng nguy cơ mắc bệnh bạch cầu ở dân số này. Đồng thời, kiểm tra sự ổn định nhiễm sắc thể đối với những trẻ khỏe mạnh mắc bệnh bạch cầu, không tìm thấy sự gia tăng bất ổn nhiễm sắc thể ở nhóm chứng hoặc nhóm quang sai do bleomycin. Một nghiên cứu so sánh với những người khỏe mạnh cho thấy rằng không có sự gia tăng số lượng dị tật bẩm sinh ở con cháu của TẤT CẢ những đứa trẻ sống lâu.
Các yếu tố di truyền và môi trường tương tác trong sự xuất hiện của ALL thời thơ ấu. Kháng nguyên bạch cầu tương thích lịch sử (HLA) được coi là một trong những yếu tố nguy cơ di truyền đối với tính nhạy cảm với bệnh bạch cầu. Mối tương quan được thể hiện trong sự gia tăng biểu hiện của các alen phổ biến nhất HLA-DR53 và HLA-DRB1 ★ 04 ở nam giới. Và ở TẤT CẢ bệnh nhân, người ta thấy rằng gen đồng hợp tử của HLA-DRB1 ★ 04 và tính đặc hiệu của HLA-DR53 đã được tăng cường đáng kể. Mối tương quan giữa gen đồng hợp tử của HLA-DRB1 ★ 04 và ALL đặc biệt nổi bật ở bệnh nhân nam. Phản ứng chéo giữa HLA-DR53 và H-2Ek được sử dụng rộng rãi bởi một số vi rút gây ung thư để bắt chước biểu mô ưu thế miễn dịch của HLA-DR53, và lượng DNA bổ sung gần gen HLA-DRB4 chứng minh rằng HLA-DRB1 ★ 04 có thể là thời thơ ấu TẤT CẢ Một trong những yếu tố di truyền. Trong nghiên cứu đối chứng allelic của DQA1 và DQB1 ở 60 trẻ bị ALL và 78 trẻ sơ sinh, người ta thấy rằng tỷ lệ mắc DQA1 ★ 0101 / ★ 0104 và DQB1 ★ 0501 ở bệnh nhân nam cao hơn so với nhóm chứng bình thường. Kết quả này gợi ý rằng có các dòng HLA nhạy cảm liên quan đến nam giới ở TẤT CẢ bệnh nhân.
Ai đó đã nghiên cứu vai trò của gen transferase và cytochrome P-450 trong các khối u ở trẻ em. Hai enzym này tham gia vào quá trình chuyển hóa các chất gây ung thư và tạo thành các yếu tố nguy cơ cao đối với nhiều loại ung thư ở người lớn, đồng thời tham gia vào quá trình biến đổi sinh học của các amin thơm trong thuốc lá, môi trường và thực phẩm thông qua N-acetyltransferase được mã hóa bởi NAT1 và NAT2. Các alen acetyl hóa nhanh và chậm này đóng một vai trò thay đổi trong nhiều loại khối u rắn trưởng thành. Hấp thu folate thấp hoặc những thay đổi trong chuyển hóa folate do kết quả của đa hình methylene tetrahydrofolate reductase (MTHFR) có liên quan đến các khuyết tật ống thần kinh và một số bệnh ung thư. Sự thay đổi tính đa hình của MTHFR dẫn đến sự gia tăng nguồn thymidine và tổng hợp DNA chất lượng cao, giúp bảo vệ sự xuất hiện của bệnh bạch cầu, đặc biệt có liên quan chặt chẽ đến bệnh bạch cầu có chuyển đoạn nhiễm sắc thể.
Wiemels và cộng sự đã báo cáo mối liên quan giữa tính đa hình MTHFR và sự sắp xếp lại gen MLL trong bệnh bạch cầu ở trẻ sơ sinh và bệnh bạch cầu ở trẻ em dương tính với TEL-AML1 hoặc tăng đơn bội. Những phát hiện này cung cấp bằng chứng cho thấy các phân nhóm sinh học phân tử khác nhau của bệnh bạch cầu ở trẻ em có thể có nguyên nhân khác nhau, và cũng cho thấy vai trò của folate trong sự xuất hiện của bệnh bạch cầu ở trẻ em. Krajinovic và cộng sự nhận thấy rằng kiểu gen trần GSTML và kiểu gen CYP1A1 có thể dự đoán một cách có ý nghĩa nguy cơ bị TẤT CẢ. Khi NAT2 bị acetyl hóa từ từ, nó thường được coi là hoạt động cùng với các kiểu gen nguy cơ cao khác như kiểu gen trần GSTML và kiểu gen CYP1A ★ 2A để làm tăng nguy cơ mắc bệnh bạch cầu. Davies và các cộng sự nhận thấy rằng kiểu gen trần GSTML là kiểu gen có ý nghĩa dự đoán về AML của trẻ em (đặc biệt là M3 và M4 trong kiểu gõ FAB). Những phát hiện này cho thấy vai trò có thể có của sự tương tác giữa gen và các yếu tố môi trường trong cơ chế bệnh sinh của bệnh bạch cầu ở trẻ em.
Gần 80% bệnh bạch cầu ở trẻ sơ sinh có kèm theo các bất thường di truyền xảy ra trên nhiễm sắc thể 11q23, tạo thành các gen dung hợp MLL. 11q23 cũng thường gặp trong bệnh bạch cầu thứ phát (AML) do chất ức chế topoisomerase II gây ra . Do đó, các học giả như Ross đã suy đoán rằng bệnh bạch cầu ở trẻ sơ sinh có thể liên quan đến các chất ức chế topoisomerase (bao gồm caffeine, trái cây và rau quả nhiều màu) tiếp xúc với điều kiện tự nhiên, và đã thực hiện một nghiên cứu đa trung tâm, và không tìm thấy topoisomerase II Mối tương quan giữa thực phẩm ức chế và tỷ lệ mắc các loại ALL. Tuy nhiên, lượng thức ăn bổ sung chất ức chế topoisomerase tăng lên có mối tương quan đáng kể với sự khởi phát của AML. Các nghiên cứu in vivo gần đây đã chứng minh rằng bioflavonoid tự nhiên có trong thực phẩm có thể gây ra sự phân cắt DNA cụ thể tại vùng điểm ngắt của gen MLL, giống như phụ gia thực phẩm. Những kết quả này cho thấy rằng việc người mẹ hấp thụ bioflavonoid có thể gây ra đứt gãy gen MLL và có thể gây chuyển đoạn nhiễm sắc thể trong tử cung, dẫn đến bệnh bạch cầu ở trẻ sơ sinh. Hút thuốc, uống rượu, dùng một số loại thuốc Trung Quốc và các loại thuốc gây tổn thương DNA và tiếp xúc với thuốc trừ sâu có thể làm tăng nguy cơ mắc bệnh bạch cầu cấp tính liên quan đến thay đổi gen MLL.
2. Khi điều tra 2117 trường hợp mắc ALL và 650 trường hợp AML trong tiền sử bệnh, người ta thấy rằng hội chứng Down, bệnh tim bẩm sinh và dị tật đường tiêu hóa thường gặp hơn ở trẻ mắc ALL; hội chứng Down, chậm phát triển trí tuệ và bệnh tim bẩm sinh phổ biến hơn ở trẻ mắc ALL. Phổ biến hơn trong AML.
3. Đặc điểm sinh học AML có cơ chế thoát khỏi quy định chết tuần tự, một số tế bào bất tử. Trong M3, rõ ràng là t (15; 17) gây ra sự hợp nhất PML / RARa, ngăn chặn sự điều hòa biệt hóa bình thường của tế bào. Kháng đa thuốc rất dễ phát triển trong điều trị AML và có nhiều cơ chế đề kháng liên quan, bao gồm P glycoprotein, được mã hóa bởi MDR trong họ gen kháng đa thuốc. Chức năng chính của nó là chủ động bơm nhiều loại thuốc vào tế bào. Cho phép các tế bào khối u kháng thuốc. Thuốc chẹn kênh canxi và cyclosporin A có thể ngăn chặn chức năng của P glycoprotein. Các bất thường nhiễm sắc thể đặc trưng phổ biến trong AML là t (8; 21) và t (3; 21) ở M2, t (15; 17) và t (11; 17) ở M3, và inv (16) ở M4Eo.
4. Phân loại hình thái Theo phân loại hình thái của Pháp, Anh và Mỹ (FAB) được công nhận nhiều hơn, AML được chia thành bảy loại từ M1 đến M7, với nhiều đặc điểm khác nhau.
1. Làm thế nào tế bào sinh ung thư và virus ung thư tế bào, bức xạ ion hóa, chất hóa học, vv gây ra bệnh bạch cầu, cơ chế chưa được hiểu đầy đủ. Sự tăng sinh, biệt hóa, già đi và chết của tế bào đều do gen quyết định, hiển nhiên sự biến đổi ác tính của tế bào cũng phải liên quan đến một số thay đổi trong gen. Hiện nay người ta đã biết rằng các tế bào động vật và người cũng như một số loại chủng vi rút có các gen khối u có thể gây ra sự biến đổi ác tính của các tế bào bình thường và cho phép chúng có được các đặc điểm sinh học mới trước đây được gọi là tế bào sinh ung thư hoặc proto-oncogenes. Chúng được gọi là sinh ung thư của virus. Các gen sinh ung là thành viên của các gen bình thường. Chúng đóng vai trò trong một thời kỳ nhất định của quá trình tăng sinh, biệt hóa, lão hóa và chết của tế bào và được điều chỉnh và kiểm soát bởi các cơ chế bên trong. Khi các gen này được kích hoạt bất thường và chuyển thành gen khối u, chúng sẽ trở thành chất gây ung thư. đang hoạt động. Các nghiên cứu đã chỉ ra rằng các tế bào sinh ung thư của virus không phải vốn có của bản thân virus, mà được chèn vào bộ gen của virus bằng cách tái tổ hợp các đoạn DNA từ tế bào chủ trong quá trình nhiễm trùng vật chủ nhiều lần .
2. Kích hoạt các gen sinh ung Sự hoạt hóa bất thường các gen sinh ung thư được chuyển thành các gen sinh ung thư, có được thông qua những thay đổi trong cấu trúc DNA của gen và rối loạn điều hòa. Bao gồm các:
(1) Đột biến điểm: Sự thay đổi một đến một số trình tự nucleotit trong chuỗi ADN của gen là đột biến điểm, ví dụ gen ung thư là đột biến gen ung thư tế bào ras;
(2) Sự sắp xếp lại nhiễm sắc thể: Những thay đổi trong cấu trúc DNA và trình tự của gen hoặc các vùng điều hòa của chúng do thay đổi chuyển đoạn, đảo đoạn, mất đoạn nhiễm sắc thể, v.v. là những cách phổ biến để kích hoạt gen sinh ung. Ví dụ điển hình là sự hình thành nhiễm sắc thể Ph, là sự hình thành chuyển đoạn t (9; 22) (q34; q11), tức là gen sinh ung thư c-ABL trên nhiễm sắc thể 9 chuyển vị trí đoạn đứt trên nhiễm sắc thể 22 và tạo thành BCR / ABL được kích hoạt bởi gen dung hợp;
(3) Khuếch đại gen: Các gen này có thể được sao chép thành nhiều bộ bản sao, một số gen tách khỏi nhiễm sắc thể để tạo thành microsome kép, một số có thể tích hợp lại vào nhiễm sắc thể, do đó sản phẩm protein tăng lên và có thể gây biến đổi tế bào ác tính.
3. Nghiên cứu về gen ức chế khối u trong những năm gần đây đã phát hiện ra rằng tế bào người có chứa gen có thể ức chế sự hình thành khối u, được gọi là gen ức chế khối u. Các gen ức chế khối u của con người được báo cáo cho đến nay bao gồm RB, P53, P16, WTI, v.v. Tốt bụng. Bởi vì đột biến và xóa gen có thể gây ra sự bất hoạt bất thường của các gen ức chế khối u, kết quả thường là sự biểu hiện quá mức của các ung thư và biến đổi tế bào. Chúng tôi đã sử dụng phân tích PCR-SSCP (đa hình dạng sợi đơn) và phép lai Southern blot để phát hiện sự xóa bỏ gen ức chế khối u P16 và đột biến điểm ở 31 trẻ em mắc bệnh bạch cầu nguyên bào lympho cấp tính . Chúng tôi nhận thấy rằng tỷ lệ xóa gen P16 (bao gồm cả đột biến điểm) ) Là 25,8%, trong đó thể đồng hợp mất đoạn: 16% đối với B-ALL, 33% đối với T-ALL và 1 trường hợp về 2 dạng đột biến điểm. Điều này cho thấy gen P16 bị bất hoạt do mất đoạn gen và đột biến điểm, có tỷ lệ mắc bệnh cao hơn trong bệnh bạch cầu nguyên bào lympho cấp, cho thấy nó có liên quan mật thiết đến sự xuất hiện, phát triển và tiên lượng của bệnh.
4. Cơ chế gây ung thư của ung thư tế bào vi rút Các vi rút gây bệnh bạch cầu tế bào T ở động vật và người trưởng thành hầu hết đều là retrovirus loại C. Sau khi xâm nhiễm vào tế bào vật chủ, chúng được tổng hợp bằng enzym phiên mã ngược và DNA polymerase sử dụng RNA của virus làm khuôn mẫu. DNA tiền virut sợi kép được tích hợp thêm vào DNA của tế bào chủ. Sau khi được tích hợp vào tế bào vật chủ, các tế bào sinh ung thư của virus có thể được kích hoạt và biểu hiện để gây ra sự biến đổi ác tính của tế bào. Chúng cũng có thể ở giai đoạn tĩnh lặng dưới sự điều hòa di truyền của tế bào vật chủ và có thể tạo ra khối u khi được kích hoạt bởi bức xạ hoặc các chất hóa học. Tác động điều hòa chuyển đổi mới được đề xuất của các sản phẩm gen virus giải thích tác dụng gây ung thư của virus HTLV-1 từ một khía cạnh khác. Có nghĩa là, một số gen của loại vi rút này có thể mã hóa một yếu tố protein đặc biệt, yếu tố này không chỉ có thể làm tăng sự sao chép của vi rút mà còn kích hoạt có chọn lọc một số gen của tế bào chủ, chẳng hạn như làm tăng tổng hợp interleukin 2 (IL-2) và thụ thể của nó. , Và sau đó thúc đẩy sự biến đổi ác tính của tế bào T.
5. Giới thiệu về quá trình tự chết Apoptosis là quá trình tự hủy diệt tế bào dưới sự hướng dẫn của gen, là cách thức thanh thải bình thường của tế bào trong quá trình hình thành phôi bình thường và sự phát triển của các mô và cơ quan trưởng thành. Khi con đường tự chết bị ức chế hoặc Sự ngăn chặn có thể làm cho các tế bào bất tử và trở thành ác tính. Quá trình tự chết bao gồm một loạt các quy định của gen. Các gen thúc đẩy quá trình chết theo quy trình bao gồm Fas, Bax, ICE, P53, v.v. và các gen ức chế quá trình chết bao gồm Bcl-2, Bcl-XL, v.v. Lý thuyết về apoptosis không chỉ mở ra một lĩnh vực mới cho việc nghiên cứu căn nguyên và bệnh sinh của bệnh bạch cầu, mà còn cung cấp những ý tưởng mới cho việc nghiên cứu bệnh bạch cầu và kháng thuốc. Nhiều loại thuốc điều trị bệnh bạch cầu, chẳng hạn như doxorubicin, cisplatin, etoposide, actinomycin D, methotrexate, cytarabine, v.v., có thể gây ra quá trình apoptosis của tế bào bệnh bạch cầu. Bộ phận của chúng tôi đã nghiên cứu hiệu ứng apoptosis của homoharringtonine gây ra các tế bào bệnh bạch cầu HL-60 và phát hiện ra rằng thuốc chủ yếu kích hoạt protein Fas và điều chỉnh giảm protein Bel-2 để bắt đầu chương trình apoptosis. Nhiều nghiên cứu về kháng thuốc đã chỉ ra rằng độ nhạy cảm của tế bào bạch cầu đối với thuốc gây apoptosis liên quan đến mức độ biểu hiện của gen Bcl-2 trong tế bào. Mức độ biểu hiện Bcl-2 càng cao thì độ nhạy càng kém. Do đó, việc phát hiện biểu hiện Bcl-2 trong tế bào bệnh bạch cầu Mức độ có thể đo độ nhạy của hóa trị và dự đoán tiên lượng.
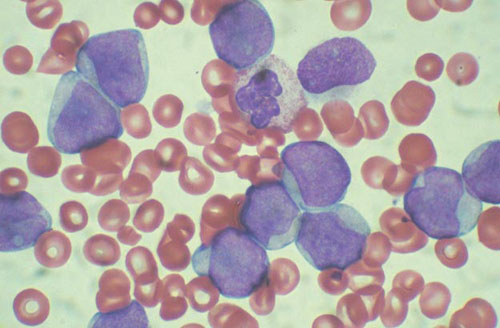

Các triệu chứng thường gặp: sốt, thiếu máu, nổi hạch, gan to, lách to, xuất huyết da và niêm mạc, nốt dưới da, gan lách to
Các biểu hiện lâm sàng của bệnh bạch cầu cấp ở trẻ em có những đặc điểm chung, chủ yếu là biểu hiện thiếu máu , xu hướng xuất huyết niêm mạc da hoặc các cơ quan nội tạng , sốt và các loại nhiễm trùng. Không giống ALL, M3 có xu hướng chảy máu nghiêm trọng hơn , và DIC dễ xảy ra trước và khi bắt đầu điều trị, trong khi thâm nhiễm nướu M5 phổ biến hơn. Ngoại trừ M4 và M5, các AML khác ít có cơ hội xâm nhập vào hệ thần kinh trung ương hơn ALL.
Ngoại trừ các mức độ khác nhau của nước da nhợt nhạt , các đốm xuất huyết và ban xuất huyết , hơn một nửa số bệnh nhân có các mức độ sưng khác nhau của gan, lá lách và các hạch bạch huyết; da và mô dưới da bị thâm nhiễm với các nốt có thể sờ thấy và nhãn cầu có thể nổi rõ khi xâm nhập quỹ đạo . Bề mặt cắt của khối sinh dục ( phần khối u ) có thể chuyển thành màu xanh lục do tác động của men myeloperoxidase có trong tế bào khối u, nên còn được gọi là ” khối u xanh “.
(1) Những người bị thiếu máu không rõ nguyên nhân, chảy máu, sốt, sốt mà không giải thích được hoàn toàn do nhiễm trùng, và các triệu chứng thâm nhiễm đa cơ quan nên được xem xét để chẩn đoán bệnh này.
(2) Những người bị thiếu máu, gan, lá lách, nổi hạch không phù hợp với mức độ chảy máu khi khám sức khỏe , đặc biệt là những người bị viêm tuyến mang tai, viêm tinh hoàn, thâm nhiễm và phì đại mô mềm, và những người có biểu hiện đau nhức xương khớp rõ rệt. Chẩn đoán bệnh.
(3) Bệnh nhân có ≥2 loạt bất thường hoặc tế bào chưa trưởng thành được tìm thấy trong máu ngoại vi nên xem xét khả năng mắc bệnh này và tiến hành thêm xét nghiệm phết tế bào tủy xương.
hình thái tế bào, kiểu miễn dịch và di truyền tế bào, đồng thời với sự phát triển cũng cần bao gồm cả phân tích kiểu gen.
(1) Hình thái tế bào tủy xương: Khi nghi ngờ bệnh bạch cầu trên lâm sàng, phải làm phết tế bào tủy xương để nhuộm hình thái và mô hóa để xác định chẩn đoán. Phôi tủy xương thường cho thấy tăng sản cao, tế bào chưa trưởng thành ≥30%, từ 30% đến 100%, khoảng 4/5 bệnh nhân có thể chẩn đoán hình thái rõ ràng sau khi nhuộm hình thái và mô hóa, 1/5 bệnh nhân khác Phân tích kiểu gen miễn dịch và di truyền tế bào là cần thiết để phân biệt thêm AML với ALL. Đặc điểm nhuộm mô hóa của từng loại AML được trình bày trong Bảng 1.
(2) Kiểu miễn dịch: Khi các tế bào gốc tạo máu của tủy xương dần dần biệt hóa và trưởng thành, chúng có thể biểu hiện các kiểu miễn dịch liên quan đến các dòng tế bào cụ thể và các giai đoạn biệt hóa. Khi kết quả hình thái tế bào và nhuộm mô hóa không nhất quán thì kiểu hình miễn dịch đóng vai trò quan trọng trong chẩn đoán . 90% bệnh nhân AML biểu hiện ít nhất một trong các CD33, CD13, CD15, CD11b và CD36. Một số kháng nguyên dòng tủy cũng được biểu hiện trên các tế bào lympho đơn thuần, vì vậy không thể chẩn đoán chỉ dựa trên kiểu miễn dịch. 4% -25% TẤT CẢ có thể biểu hiện ít nhất một kháng nguyên dòng tủy, 11% -28% AML và cả hai Kháng nguyên hệ bạch huyết.
(3) Di truyền tế bào: Các bất thường nhiễm sắc thể thường gặp và đặc trưng trong AML là t (8; 21), t (3; 21), thường gặp ở M2; t (15; 17), t (11; 17) , Phổ biến trong M3; inv (16) phổ biến trong M4Eo.
Các hạng mục giám định: phân tích hình ảnh tủy xương, phim lồng ngực, phim xương khớp tay chân, xét nghiệm máu
1. Kiểm tra máu ngoại vi cho thấy các tế bào hồng cầu và hemoglobin (Hb) giảm ở các mức độ khác nhau, số lượng bạch cầu (WBC) tăng lên đáng kể hơn một nửa, và phần còn lại có thể bình thường hoặc giảm. Lúc này còn được gọi là bệnh bạch cầu giảm tăng sinh . Tế bào bạch cầu dễ dàng nhìn thấy trong máu ngoại vi của bệnh nhân với lượng bạch cầu tăng cao, đây là bằng chứng xác thực để chẩn đoán ung thư máu. Bệnh bạch cầu không dễ nhận thấy trong máu của những người bị giảm bạch cầu hay còn gọi là bệnh bạch cầu cấp aleukemia. Có báo cáo về 1024 trường hợp TẤT CẢ trẻ em có hình ảnh máu như sau: ① Tế bào máu trắng <10 109 = “” l = “” 34 = “” 10 = “” 24 = “” 109 = “” l = “” 25 = “” 25 = ” “49 =” “109 =” “l =” “22 =” “> 50 × 109 / L chiếm 19%. ②Hb cấp <70g l = “” 44 = “” 70 = “” 110g = “” l = “” 43 = “”> 110g / L chiếm 14%. ③BPC≤20 × 109 / L chiếm 29%, (20 ~ 49) × 109 / L chiếm 23%, (50 ~ 99) × 109 / L chiếm 20% và ≥100 × 109 / L chiếm 29%.
2. Hình ảnh tuỷ xương Hầu hết hình ảnh tuỷ xương của trẻ em có độ trắng cấp tính ở lần chẩn đoán đầu tiên rõ ràng là đang hoạt động hoặc cực kỳ tích cực. Một số trường hợp cho thấy mức độ tăng sinh thấp được gọi là bệnh bạch cầu giảm tăng sinh, và sau đó có tiên lượng tốt hơn. Cho đến nay tủy đồ vẫn là cơ sở chính xác nhất để chẩn đoán độ trắng cấp, tỷ lệ tế bào nguyên thủy và chưa trưởng thành là ≥30% để chẩn đoán, ANLL cần loại bỏ vạch đỏ trước khi tính tỷ lệ này. Do sự biệt hóa và trưởng thành của các tế bào tạo máu bình thường trong tủy xương, một số lượng lớn các tế bào ung thư máu bị đình trệ ở một giai đoạn nhất định được thay thế bằng một số lượng lớn các tế bào bạch cầu vắng mặt trong một hoặc nhiều giai đoạn của quá trình trưởng thành, hiện tượng này được gọi là hiện tượng “đánh”. Các thể Auer hình que thường được nhìn thấy trong AML, đặc biệt là trong các tế bào nguyên bào, có giá trị trong việc xác định ALL. Trong những năm gần đây, người ta thấy rằng các thể phi hình que hoặc hình trục có thể được nhìn thấy trong các tế bào AML được nhuộm 3,3-diylbenzidine, và hơn 50% các hạt cấp tính có thể được phát hiện, điều này giúp ích cho việc chẩn đoán phân biệt.
3. Miễn dịch học, hóa tế bào và di truyền tế bào của các bệnh bạch cầu khác đã được đề cập trước đây. Việc sử dụng kính hiển vi điện tử truyền qua có thể giúp chẩn đoán M7 và bệnh bạch cầu cấp tính không biệt hóa. Giai đoạn cuối deoxynucleotidyl transferase (TdT) Nó giảm đáng kể trong B-ALL và AML, và tăng đáng kể trong T-ALL và C-ALL Pre-B-ALL, vì vậy nó có một ý nghĩa nhận dạng nhất định.
1. Chụp X-quang phổi kiểm tra X-quang trắng cấp tính hầu hết không đặc hiệu, X-quang phổi thường thấy hạch bạch huyết to lên , có thể thấy bóng lốm đốm khi bệnh bạch cầu xâm nhập phổi. T-ALL thường có khối trung thất.
2. Kiểm tra X-quang xương thường cho thấy loãng xương và vôi hóa, và đôi khi có phản ứng tiêu xương và màng xương khu trú . Các sọc ngang với mật độ giảm ở phần phụ của các xương dài được gọi là đường bạch cầu.


Khi chẩn đoán lâm sàng bệnh ITP, thiếu máu bất sản , giảm bạch cầu hạt , tăng bạch cầu đơn nhân nhiễm trùng , các bệnh viêm khớp khác nhau , bệnh bạch cầu thì nên nghĩ đến bệnh, khi chưa chắc chắn bệnh bạch cầu thì nên chọc tủy kịp thời. Phim xác nhận thêm chẩn đoán.
1. Phản ứng giống bệnh bạch cầu Bạch cầu máu ngoại vi tăng , tăng đáng kể và (hoặc) xuất hiện các tế bào bạch cầu chưa trưởng thành được gọi là phản ứng bệnh bạch cầu, thường do nhiễm trùng, nhiễm độc , khối u , mất máu, tán huyết, thuốc và các lý do khác. Trong các phản ứng tăng bạch cầu hạt và bạch cầu đơn nhân, thường có sự gia tăng đáng kể các tế bào bạch cầu, và có những tế bào bạch cầu chưa trưởng thành trong máu ngoại vi, nhưng điểm số phosphatase kiềm của bạch cầu trung tính trước đây tăng lên đáng kể. Bạch cầu lympho ngoại vi có thể tăng nhẹ, nhưng xuất hiện các tế bào lympho chưa trưởng thành. Nói chung, phản ứng giống bệnh bạch cầu có thể trở lại bình thường sau khi loại bỏ cảm ứng, và các tế bào hồng cầu và tiểu cầu trong máu ngoại vi của phản ứng giống bệnh bạch cầu thường không bị ảnh hưởng, và tủy xương không có những thay đổi giống như bệnh bạch cầu. Có những trường hợp không thường xuyên có phản ứng bạch cầu trên lâm sàng, khó phân biệt với ung thư máu, lúc này cần quan sát kỹ, bổ sung bằng các phương pháp miễn dịch và di truyền.
2. Thiếu máu bất sản Bệnh này có biểu hiện lâm sàng thiếu máu, xuất huyết, sốt , hình ảnh máu toàn phần giảm, có thể dễ nhầm với bệnh bạch cầu giảm tăng sinh, nhưng gan, lá lách và các hạch bạch huyết của bệnh này không sưng, tăng sản tủy xương thấp không có tỷ lệ tế bào nguyên thủy và chưa trưởng thành. Gia tăng hiện tượng.
3. Mất tế bào bào ác tính bệnh này là bạch cầu đơn nhân – hệ thống đại thực bào của rối loạn tăng sinh ác tính, có thể bao gồm sốt, thiếu máu, chảy máu, gan, lá lách và hạch bạch huyết mở rộng, thâm nhiễm trên diện rộng trên lâm sàng và hoa liễu toàn thân trở nên khó Xác định bệnh bạch cầu. Hình ảnh máu ngoại vi cũng tương tự như bệnh bạch cầu, với Hb và BPc giảm, và hơn một nửa số bạch cầu giảm, có thể tìm thấy hồng cầu chưa trưởng thành và bạch cầu hạt chưa trưởng thành, nhưng nếu tìm thấy tế bào mô ác tính thì đó là dấu hiệu cao của bệnh. Tăng sản tủy xương hoạt động hoặc giảm, hồng cầu lưới tăng và có thể nhìn thấy các tế bào mô khác nhau. Theo hình thái học, chúng có thể được chia thành các tế bào mô bất thường nói chung, tế bào mô giống bạch cầu đơn nhân, tế bào mô lympho, tế bào mô khổng lồ đa nhân và tế bào mô thực bào Nếu bạn thấy một số lượng lớn các tế bào mô thực bào và các tế bào mô bất thường nói chung, điều đó hỗ trợ cho việc chẩn đoán bệnh. Hội chứng tăng bào bào ác tính thiếu các công cụ chẩn đoán cụ thể, và hỗ trợ tủy xương không đáp ứng chẩn đoán lâm sàng không thể, và ngược lại hỗ trợ lâm sàng và những người không đáp ứng tủy xương không thể loại trừ chẩn đoán, chẩn đoán bệnh phụ thuộc vào phân tích toàn diện, tủy xương và sinh thiết hạch có thể được Cung cấp bằng chứng nhất định cho các bệnh về máu và khối u của trẻ em.
4. Bệnh tăng bạch cầu đơn nhân nhiễm trùng Bệnh này do nhiễm vi rút EB (Epstein-Barr). Trên lâm sàng thường có biểu hiện sốt, nổi mẩn ngoài da, đau thắt ngực, nổi hạch ở gan, lá lách, bạch cầu trong máu tăng chủ yếu là do tăng lympho bào, số lympho bất thường thường lên tới trên 10%. Biểu hiện lâm sàng và hình ảnh máu dễ nhầm với bạch biến cấp tính nhưng bệnh hồi phục nhanh, hình ảnh tủy đồ không có tế bào lympho nguyên thủy, có thể chẩn đoán xác định kháng thể đặc hiệu EBV như EBV-VCA-IgM.
Các hội chứng myelodysplastic (hội chứng loạn sản myelo, MDS) là một nhóm các tạo máu tổn thương tế bào gốc do loạn sản xương và rối loạn chức năng. Biểu hiện chính của bệnh này là thiếu máu, có thể kèm theo chảy máu ở nhiều mức độ khác nhau, nổi hạch ở gan, đau nhức xương trong một số ít trường hợp . MDS không chỉ nên được phân biệt với bệnh bạch cầu cấp tính, mà 20% đến 30% trường hợp cuối cùng sẽ trở thành bệnh bạch cầu cấp tính. Hình ảnh tuỷ đồ của bệnh này biểu hiện bệnh lý tạo máu 3 vạch hoặc 2 vạch hoặc một trong hai vạch. Nếu tỷ lệ vạch đỏ quá cao (> 60%) hoặc quá thấp (<5%) thì sẽ có nguyên bào vòng, nhân thùy và mảnh. Các tế bào hồng cầu như phân chia hoặc đa nhân. Các tế bào Megakaryocytes có thể xuất hiện các meganucleus nhỏ dạng lympho, các meganucleus nhỏ đơn nhân tròn, các megakaryocytes có nhiều nhân, v.v. Tế bào đơn nhân có thể thấy sự gia tăng và thay đổi hình thái của các hạt nguyên phát hoặc các tế bào đơn nhân chưa trưởng thành, nhưng tỷ lệ tế bào sơ cấp (hay tế bào đơn nhân sơ cấp) nhỏ hơn 30% nên không thể chẩn đoán là bệnh bạch cầu cấp.
Một số người ở nước ngoài đã đề xuất rằng các bước chẩn đoán của ANLL có thể được xem xét như trong Hình 1, bao gồm cả chẩn đoán phân biệt với MDS.
1. Thiếu máu và xuất huyết Tình trạng thiếu máu ngày càng nặng dần, có thể có hiện tượng hồi hộp , ù tai , tan máu và các mức độ chảy máu khác nhau. Loại M3 trên lâm sàng có xu hướng chảy máu nghiêm trọng hơn , và DIC dễ xảy ra trước và khi bắt đầu điều trị. Tụ máu dưới da và xuất huyết võng mạc có thể xảy ra , dẫn đến giảm thị lực. Chảy máu đường tiêu hóa và đường tiết niệu. Khi bị xuất huyết nội sọ , áp lực nội sọ tăng cao , biểu hiện là đau đầu, nôn , co giật và hôn mê . Đường tiêu hóa và xuất huyết nội sọ có thể gây tử vong ở trẻ em.
2. Nhiễm trùng thường phức tạp, dễ lây lan sang nhiễm trùng huyết; các vị trí nhiễm trùng thường gặp là hệ hô hấp, nhọt ngoài da , viêm ruột, viêm quanh hậu môn,… Có thể xảy ra tưa lưỡi, nấm quanh hậu môn, viêm ruột do nấm và nhiễm nấm sâu. Chờ đợi.
3. Xâm nhập tế bào bệnh bạch cầu có thể phức tạp do suy tủy xương và xâm nhập vào các mô và cơ quan toàn thân, phức tạp bởi u xanh, gan và lá lách, nổi hạch ; hội chứng tĩnh mạch chủ trên; sưng đau khớp , cản trở vận động; xâm nhập hệ thần kinh trung ương có thể phức tạp đến thần kinh trung ương Bệnh bạch cầu của hệ thần kinh có thể được biểu hiện như tăng áp lực nội sọ, mờ mắt do nhức đầu, ói mửa, và đĩa phù quang. Nó cũng có thể gây liệt mặt và tổn thương thần kinh sọ khác, ngay cả động kinh co giật, rối loạn ý thức, vv .; cả tuyến mang tai là không đau Mở rộng; Bệnh bạch cầu tinh hoàn; Thận to rõ ràng; Xâm nhập da, đường tiêu hóa, phổi, màng phổi và tim có thể gây ra các triệu chứng rối loạn chức năng cơ quan tương ứng.
Xem thêm
Bệnh bạch cầu cấp dòng lympho mãn tính ở người già nguyên nhân như thế nào? Thông tin chung về bệnh
Bệnh bạch cầu hệ thần kinh trung ương nguyên nhân như thế nào? Thông tin chung về bệnh
1. Tránh tiếp xúc với các yếu tố có hại Tránh tiếp xúc với các chất hóa học có hại, bức xạ ion hóa và các yếu tố gây ung thư máu . Khi tiếp xúc với chất độc, chất phóng xạ cần tăng cường các biện pháp bảo vệ; tránh ô nhiễm môi trường, nhất là ô nhiễm môi trường trong nhà; chú ý sử dụng thuốc hợp lý và thận trọng Thuốc độc tế bào, v.v.
2. Thực hiện tốt công tác phòng, chống các bệnh truyền nhiễm, nhất là các bệnh truyền nhiễm do vi rút, làm tốt công tác tiêm chủng .
3. Làm tốt công việc ưu sinh và ngăn ngừa một số bệnh bẩm sinh, chẳng hạn như bệnh tam nhiễm trùng 21, bệnh thiếu máu Fanconi , v.v. Tăng cường luyện tập thể dục thể thao, chú ý vệ sinh thực phẩm, giữ tâm trạng thoải mái, kết hợp làm việc và nghỉ ngơi, nâng cao sức đề kháng cho cơ thể.
Nguyên tắc điều trị AML là thuốc có hiệu quả được kết hợp với hóa trị liệu chuyên sâu, và cần chú ý đến cường độ liều dùng thuốc và cường độ thời gian dùng thuốc trong việc khởi phát bệnh và tiếp tục điều trị duy trì dài hạn liều thấp không ảnh hưởng đến tỷ lệ sống không bệnh của AML. Khi điều trị hợp lý, tỷ lệ sống 5 năm sạch bệnh là 30% -45%.
1. Liệu pháp cảm ứng Liệu pháp cảm ứng quốc tế thường được sử dụng là DA, đó là daunorubicin 40mg / m2, 1 lần / ngày × 3 ngày; Cytarabine (Ara-C) 75-100mg / lần, cứ 12 giờ 1 lần. Lần × 7 ngày. Thuốc harringtonine độc đáo của Trung Quốc cũng có hiệu quả đối với trẻ em bị AML. Nó được kết hợp với cytarabine (Ara-C) như một chương trình HA, cụ thể là (H) harringtonine 4mg / m2, 1 lần / ngày × 9 ngày; arabin Cytidine (Ara-C) 75-100mg / lần, cứ 12 giờ một lần × 7 ngày, tỷ lệ thuyên giảm cảm ứng của nó tương tự như sơ đồ DA. 80% -85% bệnh nhân mới điều trị khỏi sau 1 đến 2 liệu trình.
2. Tiếp tục hóa trị AML có thể tiếp tục sử dụng phác đồ ban đầu từ 1 đến 2 liệu trình như một phương pháp điều trị củng cố sau khi thuyên giảm. Từ những tiến bộ hiện tại, một phác đồ có chứa cytarabine liều cao (Ara-C) có thể cải thiện tiên lượng của AML. Phương pháp thường được sử dụng là cytarabine (Ara-C) 2g / m2 mỗi lần, 12 giờ một lần × 6 lần; kết hợp với daunorubicin 40mg / m2 × 2 ngày hoặc etoposide (VP-16) 160mg / m2 × 2 ngày, 1 liệu trình sau mỗi 2 đến 3 tuần, 3 liệu trình liên tiếp sau khi điều trị củng cố như điều trị chuyên sâu. Không giống như AML, ALL yêu cầu hóa trị duy trì liều thấp lâu dài hơn, nhưng trong AML, hóa trị ức chế tủy liên tục là bắt buộc . Nếu tiếp tục hóa trị cho đến khoảng 12 tháng, có thể ngừng thuốc. Kéo dài hóa trị không cải thiện tiên lượng. Có thể hóa trị liên tục. Thay thế HA, DA và cytarabine (Ara-C) liều cao. Chú ý đến liều tích lũy của thuốc chống khối u anthracycline trong toàn bộ thời gian điều trị , thường được kiểm soát dưới 350mg / m2.
Tretinoin (axit retinoic all-trans) có hiệu quả chống lại M3 và có thể tạo ra sự biệt hóa và trưởng thành của nó. 60% đến 70% bệnh nhân có thể thuyên giảm sau khi sử dụng tretinoin một mình, nhưng họ vẫn tái phát mà không cần hóa trị. Hiện nay, người ta chủ trương bắt đầu hóa trị liệu cảm ứng AML sau 3-10 ngày tretinoin cho bệnh nhân M3, và tiếp tục hóa trị liệu theo AML. Việc áp dụng tretinoin có thể làm giảm đáng kể tỷ lệ mắc bệnh DIC do hóa trị liệu gây ra. Tác dụng của hóa trị liệu kết hợp với tretinoin đối với khả năng sống sót khỏi bệnh tốt hơn so với hóa trị liệu đơn thuần. Tretinoin được dùng ngắt quãng sau khi thuyên giảm, chẳng hạn như cứ 2 ~ Từ 7 đến 14 ngày trong 3 tháng vẫn thực hiện hóa trị theo AML.
3. Ngăn ngừa xâm nhập hệ thần kinh trung ương Đối với M4 và M5, hóa trị trong lớp tương tự như ALL là cần thiết để ngăn ngừa xâm nhập hệ thần kinh trung ương. Cách sử dụng được thể hiện trong Hình 2. Người ta vẫn còn tranh luận về việc liệu các AML khác có cần được ngăn chặn hay không.
4. Tiên lượng của ghép tủy xương đối với AML xấu hơn đáng kể so với ALL, đặc biệt là đối với những người có yếu tố nguy cơ cao. Do đó, nếu những bệnh nhân này có những người hiến tặng gia đình có liên quan phù hợp với HLA thì nên cân nhắc ghép tế bào gốc tạo máu toàn thể . Việc cấy ghép tế bào gốc tạo máu tự thân có hiệu quả hay không vẫn còn gây tranh cãi, và hầu hết chúng được ghi nhận là không khác gì so với hóa trị liệu thông thường.
5. Tái phát và thoái lui AML rất khó điều trị sau khi tái phát, nhất là đối với những người tái phát trong thời gian điều trị, nếu có thể thuyên giảm thì phải phấn đấu ghép tế bào gốc tạo máu toàn thể trong thời gian ngắn, vì thời gian lui bệnh thường ngắn.
(2) Tiên lượng
Các yếu tố bất lợi được công nhận nhiều hơn ảnh hưởng đến tiên lượng của AML bao gồm:
1. Tổng số lượng bạch cầu lúc khởi phát> 100 × 109 / L.
2. AML là khối u thứ hai.
3. Di truyền học tế bào cho thấy đơn bội 7, và AML được biến nạp từ MDS.
Ngoài ra, các bệnh lý to, M4 hoặc M5, không thuyên giảm sau 1 đợt điều trị cũng được coi là những yếu tố bất lợi ảnh hưởng đến tiên lượng bệnh.
Chế độ ăn cho trẻ bị bệnh bạch cầu cấp tính không phải lympho
Bệnh nhân ung thư máu đến chế độ ăn nhiều đạm, nhiều vitamin, sốt cao chế độ ăn uống dễ tiêu hóa, ăn nhiều trái cây tươi, rau xanh, bổ sung vitamin, ăn cay, có thể ăn nhiều cam, cam, táo, dưa đỏ, dưa hấu, chanh Nho, bưởi, dâu tây, dứa và các loại trái cây khác; quả óc chó, hạt thông, quả hồ trăn, vừng, hạnh nhân, quả óc chó, hạt dưa, ngô, lúa mì, v.v …; ngoài ra, nấm và tỏi được công nhận là loại rau có tác dụng ức chế ung thư và có thể ăn được nhiều hơn.