Bệnh Toxoplasmosis là bệnh gì? Làm sao để phát hiện ra bệnh?
8 Tháng Mười Hai, 2020Contents 1, Bệnh Toxoplasmosis là bệnh gì? Bệnh Toxoplasmosis, còn được gọi là bệnh toxoplasma , là một bệnh...
Contents
B viêm gan virus (viêm gan siêu vi loại B, bệnh viêm gan B cho ngắn) hệ thống là do virus viêm gan B (HBV), để mệt mỏi , chán ăn , buồn nôn , nôn , mệt mỏi của dầu, gan và rối loạn chức năng gan như những biểu hiện lâm sàng chính.

Một số trường hợp Bệnh viêm gan B bị sốt và vàng da ; trong một số trường hợp, bệnh diễn biến chậm và trở thành mãn tính, hoặc phát triển thành xơ gan hoặc thậm chí ung thư gan; những trường hợp nặng có thể tiến triển thành viêm gan nặng với tiến triển nhanh chóng; những trường hợp khác trở thành người mang virus không có triệu chứng.
Bệnh viêm gan B lây lan qua máu và dịch cơ thể và có trạng thái mang mầm bệnh mãn tính. Vì có thể lây nhiễm qua đời sống tình dục nên nó được xếp vào danh sách các bệnh lây truyền qua đường tình dục trên toàn thế giới.
Bệnh viêm gan B phổ biến ở Trung Quốc, và tỷ lệ lây nhiễm trong dân số cao, với tỷ lệ lây nhiễm lên đến hơn 35% ở một số khu vực. Viêm gan B, bệnh lao và AIDS là một trong những bệnh truyền nhiễm phổ biến nhất trên thế giới.
Bệnh viêm gan B là nguyên nhân gây tử vong đứng hàng thứ 10 trên thế giới, khoảng 350 đến 400 triệu người trên thế giới bị nhiễm vi rút viêm gan B, con số này gấp 8 lần số người nhiễm AIDS.
Bệnh viêm gan B ban đầu là nhiễm độc gan . Virus viêm gan B có khả năng kháng thuốc rất cao, rất khó để tiêu diệt nó ở nhiệt độ 60 ° C, nó có thể tồn tại khoảng 7-8 phút ở nhiệt độ cao 100 ° C.
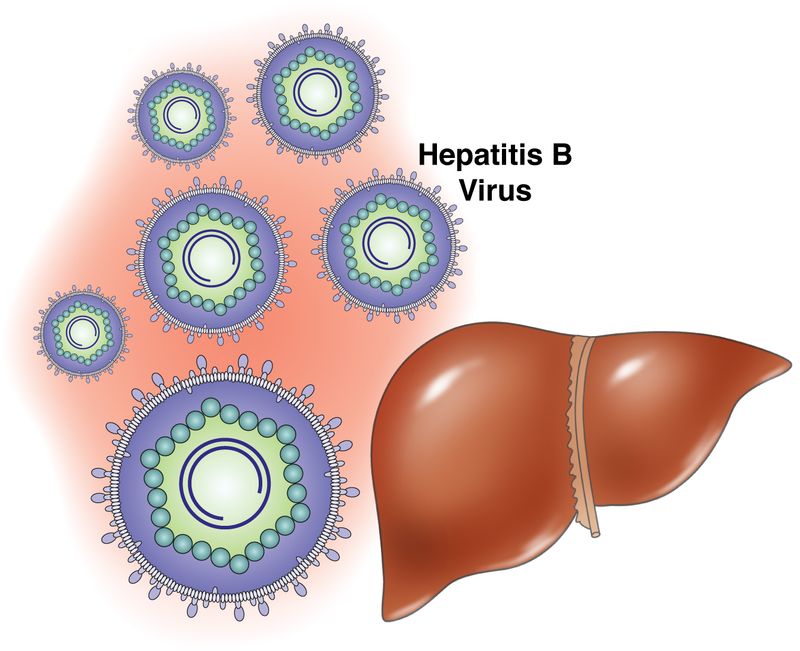

Trong số các loại viêm gan, thời gian ủ bệnh của virus viêm gan B là lâu nhất, từ 4 – 22 tuần.
Virus bệnh viêm gan B tồn tại và nhân lên trong tế bào gan. Sau đó nó được bài tiết vào máu, do đó không chỉ vi rút cao trong máu mà hầu hết các tế bào gan đều bị nhiễm bệnh.
Bản thân virus bệnh viêm gan B không trực tiếp gây ra các tổn thương ở tế bào gan mà chỉ tồn tại và nhân lên trong tế bào gan, kháng nguyên nhân lên được biểu hiện trên màng tế bào gan, giúp kích thích hệ miễn dịch của cơ thể nhận biết và loại bỏ chúng.
Sau khi cơ thể con người nhiễm virus viêm gan B, diễn biến của bệnh cũng khác nhau do chức năng miễn dịch khác nhau.
Nếu chức năng miễn dịch của cơ thể hoạt động tốt, hệ thống miễn dịch sẽ nhận biết virus viêm gan B sau khi được kích hoạt, tấn công các tế bào gan đã bị nhiễm virus và loại bỏ nó, dẫn đến viêm gan B cấp tính; nếu chức năng miễn dịch của cơ thể được kích hoạt nhưng ở trạng thái thấp.
Tế bào gan bị nhiễm vi-rút bệnh viêm gan B tấn công nhiều lần nhưng không thể loại bỏ chúng hoàn toàn, dẫn đến các đợt viêm mô gan mãn tính lặp đi lặp lại. Đây là bệnh viêm gan B mãn tính; nếu chức năng miễn dịch của cơ thể ở trạng thái dung nạp, nó không thể nhận ra vi-rút viêm gan B
Vì vậy nó sẽ không tấn công người bị nhiễm bệnh. Tế bào gan, vi rút và con người “chung sống hòa bình”, đây là vật mang vi rút viêm gan B.
Virus bệnh viêm gan B (HBV) là một hạt hình cầu (hạt Dane), đường kính 42-47 nm, bao gồm vỏ và lõi. Vỏ có nhiều hạt nhỏ hình cầu, chỉ chứa kháng nguyên bề mặt virus (HBsAg). Lõi chứa axit deoxyribonucleic sợi đôi hình tròn (DNA), DNA polymerase, kháng nguyên lõi (HBcAg) và kháng nguyên e (HBeAg).
Sợi dương của DNA sợi kép ngắn và không hoàn chỉnh, chiều dài chỉ bằng 50% sợi âm, không chứa khung đọc mở và không thể mã hóa protein. Sợi âm hoàn chỉnh, có chiều dài không đổi, chứa khoảng 3200 nucleotit, có 4 khung đọc mở lớn, có thể mã hóa tất cả các protein của virus: gen vùng
①S. Mã hóa protein áo virus (HBsAg), được chia thành các vùng gen S, pre-S1 và pre-S2 cùng mã hóa ba peptit protein áo, nghĩa là, protein chính được mã hóa bởi gen S, protein giữa được mã hóa bởi gen trước S2 và S, và protein lớn được mã hóa bởi pre Các gen S1, trước S2 và S mã hóa. Chức năng và đặc tính của các protein ba lớp áo là khác nhau;
②C. Mã hóa protein kháng nguyên lõi và kháng nguyên e thành phần hòa tan của nó, vùng tiền C có thể đóng một vai trò trong việc lắp ráp và bài tiết gen HBV;
③P. Sản phẩm dịch mã là DNA polymerase của virus; gen ④X. Trong mã hóa HBxAg, HBsAg hoặc HBcAg hiện diện trong bệnh STD nam trong nhân gan, có thể là một protein điều hòa phiên mã.
Có ba loại hạt virus khác nhau trong huyết thanh của người nhiễm HBV, đó là các hạt hình cầu nhỏ (đường kính 22nm), hạt hình ống (đường kính 22nm, chiều dài 100-1000nm) và hạt Dane (đường kính 42nm).
Hai loại đầu tiên là protein áo HBV dư thừa và các hạt rỗng hoặc không hoàn chỉnh, không có khả năng lây nhiễm. Chỉ các hạt Dane mới nhân lên trong tế bào gan và có khả năng lây nhiễm.
Tinh tinh và khỉ lao là những động vật mẫn cảm. HBV có thể phát triển trong tế bào thận người, thận khỉ và tế bào màng ối của người. HBcAg có thể được phát hiện từ môi trường nuôi cấy mô nói trên và gây ra những thay đổi tế bào.
Khả năng kháng HBV rất mạnh, đun sôi trong 30 phút 121 pressure hơi nước áp suất cao 15 phút 160 heat nhiệt khô trong 2 giờ, ethylene oxide 1,6g / L45 phút, 0,5% natri dichloroisocyanurat 30 phút, 0,5% iốt trong 10 phút, 2% glutaraldehyde kiềm, 0,5 % Axit peracetic có thể bị bất hoạt trong 7 phút.
Cồn, muối amoni bậc bốn và chlorhexidine không dễ bị bất hoạt. 30 phút bức xạ tia cực tím có thể tiêu diệt HBV.
Các kiểu phụ HBsAg và ý nghĩa của chúng: Các kiểu phụ HBsAg “a” là phổ biến, các kiểu phụ d và y, w và r là các alen của nhau, vì vậy nó được chia thành 4 kiểu phụ chính: adw, adr, ayw Và ayr.
Kiểu con W có thể được chia thành W1, W2, W3 và W4. Sự phân bố của các phân nhóm HBsAg thay đổi theo khu vực, thời gian và dân tộc. Quốc tịch Hán ở Trung Quốc chủ yếu là adr, sau đó là adw; các dân tộc thiểu số chủ yếu là ayw, và ayr rất hiếm.
Ứng dụng của nghiên cứu kháng thể đơn dòng phân nhóm đã chứng minh rằng d và y, w và r có thể cùng tồn tại trên cùng một hạt kháng nguyên, tạo thành các phân nhóm phức tạp như adwr, aywr, adyw hoặc adyr.
Trong số các phân nhóm của HBsAg, mặc dù có một miễn dịch chéo nhất định do nhóm các yếu tố quyết định kháng nguyên “a”, nhưng miễn dịch chéo này là không đầy đủ.
HBV gây bệnh cấp tính ở những người bị nhiễm có chức năng miễn dịch bình thường; viêm gan mãn tính và bệnh gan mãn tính xảy ra ở những người có chức năng miễn dịch bất thường .

HBV không phải là virus gây bệnh tế bào, sau khi nhiễm HBV, phản ứng miễn dịch của vật chủ phải gây bệnh và làm cho bệnh tiến triển.
(1) Yếu tố miễn dịch:
Đáp ứng miễn dịch đối với kháng nguyên virut trong quá trình nhiễm virut viêm gan có liên quan đến quá trình đào thải và sinh bệnh của virut.
Khi bị nhiễm HBV, phản ứng của kháng thể dịch thể với kháng nguyên màng ngoài giúp loại bỏ các phần tử vi rút trong máu; phản ứng miễn dịch tế bào đối với kháng nguyên nucleocapsid và sao chép loại bỏ vi rút và làm tổn thương tế bào gan.
① Thanh thải miễn dịch vi rút và tổn thương miễn dịch mô gan Phản ứng miễn dịch tế bào của vật chủ đối với kháng nguyên vi rút trên bề mặt tế bào gan thường được coi là yếu tố quyết định tổn thương tế bào gan.
Đáp ứng miễn dịch tế bào cho thấy sự xâm nhập của các tế bào đơn nhân trong các mô gan, sau đó là sự phá hủy mô ở các mức độ khác nhau; sự phá hủy mô cũng liên quan đến miễn dịch dịch thể, có thể do sự hình thành các kháng thể phản ứng, kháng thể và bổ thể, hoặc phức hợp miễn dịch và trong mô Sự lắng đọng.
Lý do cho sự kéo dài của nhiễm vi rút viêm gan là do đáp ứng miễn dịch thấp đối với kháng nguyên vi rút, thường là do sự thoát miễn dịch sau khi vi rút đột biến; khả năng dung nạp miễn dịch ở trẻ sơ sinh đóng một vai trò quan trọng trong sự tồn tại của nhiễm HBV.
Tế bào T trong gan: Một số lượng lớn tế bào lympho nhạy cảm từ bệnh nhân CHB (viêm gan B mãn tính) xâm nhập vào gan. Máu ngoại vi chỉ có thể phản ánh một phần quá trình miễn dịch xảy ra trong gan.
Những tế bào có khả năng sao chép tốt hơn những tế bào không có sự sao chép. CD4 / Tỷ lệ tế bào CD8 cao hơn đáng kể, cho thấy rằng tế bào T CD4 cảm ứng trợ giúp tại chỗ có thể được kích hoạt bởi HBcAg và điều hòa tích cực hoạt động gây độc tế bào của CD8CTL.
Gần 70% dòng tế bào Th được phân lập từ các tổn thương hoạt động là tế bào Th1, trong khi chỉ có 4% PBMC. Mật độ Th1 trong quần thể tế bào CD4 trong khoang nội gan càng lớn thì mức IFNγ được tạo ra càng cao và hoạt tính gây độc tế bào càng mạnh.
Kích thích kháng nguyên trong môi trường viêm ở gan có thể tạo điều kiện cho các tế bào này mở rộng. Tế bào Th1 tham gia vào cơ chế gây tổn thương tế bào gan của CHB.
Sự nhận biết đặc hiệu của kháng nguyên: Sự khởi đầu của một phản ứng miễn dịch đặc hiệu là sự nhận biết của kháng nguyên đích bởi phức hợp thụ thể tế bào T.
Phức hợp thụ thể tế bào T (sự kết hợp TCR và CD3 trên màng tế bào lympho) cũng bao gồm các kháng nguyên và các chất quyết định MHC trên bề mặt của tế bào trình diện kháng nguyên hoặc tế bào đích.
Enzim nucleocapsid protein của kháng nguyên nucleocapsid của HBV chỉ là một đoạn nhỏ của oligopeptide (peptit epipeptit) gồm 8-16 axit amin được xử lý nội bào.
Các vị trí nhận biết của tế bào T CD4 gần như nằm trong các biểu mô AAl-25 và AA61-85 của peptit HBc / eAg; các vùng trình tự được CD8CTL nhận ra không được xác định đầy đủ.
Tế bào T thuộc các chủng tộc khác nhau và các phân nhóm nhiễm MHC khác nhau nằm trong nucleocapsid Các epitope nhận biết trên trình tự axit amin của kháng nguyên là khác nhau.
IgG-anti-HBc có thể che lấp một phần sự biểu hiện của HBcAg, và anti-HBc ức chế sự nhận biết kháng nguyên đích của HBV bằng CTL, đây là một trong những yếu tố làm cho nhiễm HBV kéo dài.
Anti-HBc có thể ức chế tác dụng gây độc tế bào trên tế bào gan, và anti-HBc do người mẹ đưa vào thụ động cũng có thể có tác dụng tương tự.
Hạn chế HLA (kháng nguyên bạch cầu): Phức hợp oligopeptide / HLA-Ⅱ kháng nguyên được trình bày bởi APC (tế bào trình diện kháng nguyên) có thể liên kết trực tiếp với vùng cấu trúc β2 của các phân tử CD4 / HLA-Ⅱ của tế bào T CD4, do đó hạn chế ảnh hưởng và Tính đặc hiệu của sự tương tác giữa các tế bào đích.
Màng tế bào gan của những bệnh nhân bị bệnh gan hoạt động có biểu hiện HLA-I mạnh, có thể cung cấp các oligopeptide nucleocapsid cho tế bào T. hiệu quả hơn.
Tương tự, peptide kháng nguyên trong APC kết hợp với HLA-II để tạo thành một phức hợp, phức hợp này được trình bày trên bề mặt tế bào.
Tế bào Th sử dụng các phân tử CD4 trên bề mặt của chúng để phát hiện HLA-II trên bề mặt của APC và sử dụng TCR của chúng để phát hiện các peptit kháng nguyên bổ sung trong rãnh. Đây là quá trình nhận dạng của tế bào CD4Th.
Liên kết giữa TCR và phức hợp peptit / HLA không ổn định, và phân tử CD4 phải kết hợp với phân đoạn β2 của HLA-Ⅱ, và phân tử CD8 phải kết hợp với phân đoạn α3 của HLA-I để tạo thành cấu trúc ba chiều để duy trì.
Thời gian tiếp xúc cần thiết giữa TCR và tổ hợp. Ngoài ra, các tế bào này đều tạo ra các phân tử kết dính tế bào, và sự kết dính giữa các tế bào sẽ tăng cường phản ứng giữa các tế bào.
Cơ sở của di truyền miễn dịch thể hiện trong MHC (phức hợp tương hợp mô chính) là một yếu tố quan trọng hạn chế sự phát triển của nhiễm HBV, và có thể giải thích sự khác biệt về sắc tộc trong tính nhạy cảm với HBV.
Đã có nhiều báo cáo về mối tương quan giữa định kiến HLA và kinh nghiệm lâm sàng ở bệnh nhân nhiễm HBV, nhưng chưa có sự thống nhất.
Các khuôn mẫu HLA có liên quan tích cực đến hoạt động mãn tính của nhiễm HBV là A3-B35, A29, A2, B8, B35, DR3, DR7, và liên quan tiêu cực đến B5, B8, DQwl, DR2 và DR5.
Cytokine: Cytokine truyền thông tin miễn dịch giữa các tế bào, tạo thành một mạng lưới cytokine điều hòa miễn dịch với nhau, qua đó các phản ứng miễn dịch của tế bào được thực hiện.
Trong bệnh viêm gan cấp tính, IFN được tạo ra trong vùng bị nhiễm, và các tế bào gan bị nhiễm sẽ giải phóng IFN ra môi trường xung quanh, dẫn đến tình trạng kháng virus của các tế bào gan lân cận.
Trong viêm gan mãn tính, các cytokine được giải phóng tại chỗ bằng cách thâm nhập vào các tế bào đơn nhân hoặc các tế bào không nhu mô khác có vai trò trong phản ứng miễn dịch, tăng sinh tế bào và xơ hóa.
IL-2: Th sản xuất IL-2 và biểu hiện IL-2R, là liên kết trung tâm trong việc điều hòa miễn dịch tế bào và miễn dịch dịch thể.
Trong bệnh viêm gan mãn tính và bệnh gan mãn tính, việc sản xuất IL-2 bị giảm, và việc bổ sung IL-2 ngoại sinh không thể được điều chỉnh, cho thấy rằng sự biểu hiện của IL-2R cũng bị giảm, và IL-2 bị giảm không thể được sử dụng đầy đủ và do đó không thể được kích hoạt hoàn toàn.
Tăng sinh tế bào đặc biệt rõ rệt trong CHB và suy gan. Chức năng tế bào sát thủ hoạt hóa lymphokine (LAK) gây ra IL-2 cũng bị giảm.
Interferon: Trong trường hợp viêm gan cấp tính, các tế bào gan bị nhiễm sẽ giải phóng IFN ra môi trường xung quanh, gây ra tình trạng kháng virus của các tế bào gan liền kề.
Khả năng sản xuất IFN bị giảm khi nhiễm HBV mãn tính, và thấp nhất ở bệnh nhân suy gan. Trong huyết thanh của bệnh nhân có chất ức chế IFN.
Yếu tố hoại tử khối u α: chủ yếu được sản xuất bởi bạch cầu đơn nhân và đại thực bào, TNF-α; có thể tăng cường sự biểu hiện của nhiều loại phân tử kết dính, gây viêm và tác dụng độc tế bào. TNF-α; có thể đầu độc các tế bào, đặc biệt có thể kích hoạt các tế bào miễn dịch gây độc tế bào.
Yếu tố tăng trưởng biến đổi α: Được đặt tên vì nó có thể biến đổi kiểu hình của nguyên bào sợi bình thường, các tế bào T và B hoạt hóa có thể tạo ra một lượng TGFβ lớn hơn. Nói chung, TGFβ kích thích các tế bào có nguồn gốc từ trung bì và ức chế các tế bào có nguồn gốc từ tế bào biểu mô.
Thêm TGF-β1 vào PBMC (tế bào đơn nhân máu ngoại vi) của bệnh nhân CHB: nó có tác dụng ức chế đáng kể IFN-γ và anti-HBc do HBcAg kích thích.
Nó làm giảm sự tăng sinh của PBMC do HBcAg kích thích. TGF-β không có sự khác biệt rõ ràng về tác dụng ức chế đối với miễn dịch tế bào hoặc thể dịch, miễn dịch tế bào hoặc dịch thể, miễn dịch đặc hiệu hoặc không đặc hiệu với kháng nguyên
Nó có thể ức chế tế bào T, tế bào B và bạch cầu đơn nhân; nó cũng có thể ức chế CTL hạn chế HLA-I và nó có thể ức chế nhiễm HBV Hoạt động gây độc tế bào của tế bào gan.
TGF-β; 1 kích hoạt các tế bào dự trữ chất béo ở gan sản xuất protein nền và tạo ra sự tổng hợp collagen và các thành phần chất nền ngoại bào khác. Phổ cytokine trong gan
Các cytokine loại Th1 bao gồm IL-2, IFN-γ và TNF-β, chủ yếu tham gia vào miễn dịch tế bào; các cytokine loại Th2 như IL-4 và IL-5, chủ yếu điều chỉnh các đáp ứng miễn dịch dịch thể.
Các tế bào thâm nhiễm ở gan CHB và CHC (viêm gan C mãn tính) có các loại cytokine khác nhau, cho thấy các hành vi đáp ứng miễn dịch kháng virus khác nhau.
Trong CHC, đáp ứng Th1 chiếm ưu thế và ức chế sự nhân lên của HCV (virus viêm gan C), nhưng không đủ để loại bỏ hoàn toàn nó, do đó, nhiễm HCV luôn ở mức tải lượng virus thấp.
Trong CHB, phản ứng Th2 mạnh hơn và Th1 yếu hơn chỉ có thể duy trì tác dụng kháng vi-rút hiệu quả thấp, do đó nhiễm trùng có xu hướng kéo dài.
Như đã đề cập ở trên, tổn thương mô gan do nhiễm HBV bắt đầu với phản ứng của tế bào T kháng nguyên đặc hiệu, sau đó là tương tác với cytokine do các tế bào viêm không đặc hiệu tạo ra.
Một chất trung gian quan trọng của viêm là TNF IFN-γ kích thích sản xuất TNF-α trong CHB hoạt động, trong khi hầu như không có sản xuất TNF-α trong AsC. Ngoài ra, sự gia tăng sản xuất IL-1 trong CLD có liên quan đáng kể đến lượng xơ hóa trong sinh thiết gan.
Ở những bệnh nhân đáp ứng hoàn toàn với điều trị bằng interferon, tình trạng viêm được kích hoạt từ 8 đến 10 tuần sau khi bắt đầu điều trị, và PBMC thường tạo ra TNF-α và IL-1 cùng lúc; những yếu tố này không tăng ở những bệnh nhân không đáp ứng với điều trị.
Tại đây, tế bào lympho T kết nối hai hệ thống thông qua lymphokine IFN-γ và đơn nhân Mφ thông qua các yếu tố đơn nhân TNF-α và IL-1.
② Miễn dịch chống virus và nhiễm virus dai dẳng: Phần chính của bảo vệ miễn dịch là kháng nguyên màng ngoài của virus.
Đáp ứng kháng thể màng ngoài: Anti-HBs dễ dàng được phát hiện trong giai đoạn phục hồi sau khi loại bỏ vi rút, và không xuất hiện trong các trường hợp nhiễm trùng mãn tính, vì vậy nó là một kháng thể trung hòa; và có thể ngăn chặn vi rút bám vào và xâm nhập vào các tế bào nhạy cảm.
Tuy nhiên, anti-HBs cũng liên quan đến sự xuất hiện của một số hội chứng ngoài gan liên quan đến nhiễm HBV bằng cách hình thành phức hợp kháng nguyên-kháng thể.
Dung nạp miễn dịch: Dung nạp miễn dịch là trạng thái không đáp ứng miễn dịch được tạo ra bởi hệ thống miễn dịch sau khi tiếp xúc với một kháng nguyên nào đó và chỉ đặc hiệu với kháng nguyên đó.
Sự dung nạp miễn dịch đối với HBV xảy ra phổ biến hơn ở trẻ em bị nhiễm bệnh. Nó tạo thành cơ sở miễn dịch của AsC.
Các cơ chế có thể có của khả năng dung nạp miễn dịch: A. Tế bào miễn dịch có một số lượng lớn các dòng tế bào với các đặc tính khác nhau. Các dòng tế bào tương ứng với HBsAg trong thời kỳ sơ sinh tiếp xúc với các yếu tố quyết định HBsAg, thay vì đáp ứng miễn dịch, chúng sẽ bị loại bỏ hoặc ức chế; B.
Việc thiếu phản ứng với anti-HBs do chức năng tăng cường của CD8T; C. HBeAg của mẹ có khả năng dung nạp miễn dịch đối với nhiễm HBV ở trẻ sơ sinh; D.
Nồng độ kháng nguyên cao trong huyết thanh làm cạn kiệt các tế bào B nhân bản cụ thể và một lượng nhỏ kháng thể được tạo ra có thể bị tiêu thụ bởi một lượng lớn kháng nguyên; Hoặc CTL kháng vi-rút bị cạn kiệt do lượng vi-rút cao.
Nhiễm trùng dai dẳng: A. Đột biến vi rút: thoát miễn dịch do đột biến; B. Nhiễm trùng vẫn còn tại vị trí miễn dịch: một số mô ngoài gan bị nhiễm vi rút khó tiếp cận hoặc một số loại tế bào không biểu hiện phân tử HLA.
Nếu vi rút có thể Sự nhân lên ở những bộ phận này có thể thoát khỏi sự thanh thải miễn dịch và trở thành nguồn gốc của nhiễm trùng gan dai dẳng; C. Dung nạp miễn dịch: Hầu hết bệnh nhân nhiễm HBV mãn tính có mức độ dung nạp miễn dịch khác nhau.
(2) Sự thanh thải vi rút apoptosis của tế bào gan và tổn thương mô chủ yếu là do hoại tử tế bào của CTL qua con đường perforin hoặc quá trình chết của tế bào qua CD95L;
Cũng có thể các đại thực bào monocyte trải qua quá trình apoptosis hoặc hoại tử qua con đường TNF-α. Cả hai đều có cơ chế độc lập và nguồn gốc khác nhau. Apoptosis là một hình thức chết tế bào chủ động, còn hoại tử là một hình thức thụ động.
Apoptosis là một hình thức chết tế bào cụ thể khác với hoại tử tế bào về nhiều mặt hình thái và sinh hóa, nhưng cả hai đều có một số phần hành động chung, ngăn cách hai ranh giới. Nó không rõ ràng.
CD95L và CD95, hoặc FasL và Fas, là các phân tử bề mặt tế bào của nhiều tế bào. CD95L là phối tử và CD95 là thụ thể của nó. CD95L được biểu hiện bằng CTL kết hợp với CD95 được biểu hiện bởi tế bào đích có thể gây ra quá trình apoptosis của tế bào đích.
TNF-α và TNR-β: TNF-α chủ yếu được sản xuất bởi Mφ. Nó là một cytokine hướng màng phổi hoặc toàn màng phổi và đóng một vai trò quan trọng trong viêm và sốc nhiễm trùng .
CD95L: CD95L trên CTL liên kết với CD95 trên tế bào đích, do đó kích hoạt chương trình tự sát bên trong tế bào đích.
Tín hiệu qua CD95 dẫn đến quá trình apoptosis, và việc kích hoạt con đường này yêu cầu liên kết chéo của CD95 với kháng thể hoặc phối tử của nó.
Con đường chết được kích thích bởi CD95 không dựa vào Ca2 ngoại bào, cũng như không đòi hỏi sự tổng hợp của các phân tử lớn.
Tác dụng gây độc tế bào của CTL phụ thuộc IL-2, do đó, IL-2 có thể ức chế sự xuất hiện của quá trình apoptosis.
Màng tế bào của tế bào apoptotic còn nguyên vẹn, phân mảnh thành các thể apoptotic và bị nuốt chửng bởi Mφ hoặc các tế bào gan lân cận, virus và các chất khác không bị rò rỉ, đó là cơ chế tự bảo vệ.
Virus DNA đối kháng với quá trình apoptosis của tế bào. Tế bào HepG2215 được chuyển nhiễm HBV có khả năng chống lại sự kích thích của các yếu tố apoptotic hơn các tế bào HepG2 không được truyền nhiễm.
Tế bào gan của bệnh viêm gan siêu vi và tế bào u gan của HCC liên quan đến HB cũng biểu hiện CD95L. “Tự sát” và “giết chết sib” của tế bào gan là một cuộc tấn công không miễn dịch để loại bỏ vi rút, đây có thể là cơ chế bù trừ cho HBV để đối kháng với quá trình chết theo chương trình.
TNF-α: chủ yếu do Mφ tạo ra, và độc tính tế bào qua trung gian của nó phụ thuộc vào độ nhạy của tế bào đích. Khi chất ức chế dịch mã cycloheximide nhạy cảm với tế bào, TNF-α gây ra quá trình apoptosis, đây là đặc điểm điển hình của quá trình apoptosis.
Tế bào gan trong bệnh viêm gan virus cũng tạo ra TNF-α, và HBx có thể biến đổi và hoạt hóa promoter TNF-α; việc giết chết TNF-α phụ thuộc vào mức độ biểu hiện của HBV và TNF-α có thể gây ra apoptosis ở các dòng tế bào biểu hiện cao.
A. Viêm gan nặng cấp tính và cấp tính: Trong sinh lý bệnh của quá trình chết tế bào gan do virus gây ra, hiện tượng chết rụng và hoại tử thường xảy ra đồng thời.Có một mô hình chuột để minh họa sự phát triển của bệnh viêm gan nặng cấp tính.
Những con chuột chuyển gen HBsAg được tiêm CTL đặc hiệu với HBsAg, và các tổn thương phát triển theo từng giai đoạn: trong vòng 4 giờ, sự tương tác trực tiếp giữa CTL và tế bào gan đã kích thích một số lượng nhỏ tế bào gan có HBsAg dương tính trải qua quá trình apoptosis, và các cơ thể apoptotic lan rộng xuất hiện;
4-12 giờ Tế bào gan apoptotic tiếp tục tăng, và nhiều tổn thương viêm xuất hiện, trộn lẫn với một số lượng lớn các tế bào lympho và bạch cầu trung tính không đặc hiệu với kháng nguyên, làm tăng tác dụng tế bào tại chỗ của CTL;
24 đến 72 giờ sau khi tiêm, hầu hết các tế bào gan trở nên thoái hóa giống như bong bóng , Hoại tử phân bố rộng khắp tiểu thùy, có nhiều tế bào apxe. CTL được kích thích bởi kháng nguyên để tiết IFN-γ; nó kích hoạt các tế bào viêm không đặc hiệu,
Bao gồm Mφ trong gan, và làm tăng hiệu ứng tế bào của CTL và gây hoại tử tế bào gan lớn . Do đó, viêm gan nặng cấp tính xảy ra sau khi CTL giới hạn HBsAg và MHC-I nhận ra kháng nguyên, tiết IFN-γ, và kích hoạt Mφ.
TNF-α; có thể tiêu diệt các dòng tế bào khối u khác nhau thông qua hoại tử hoặc apoptosis (tùy thuộc vào hệ thống thí nghiệm).
Có hai giai đoạn tổn thương gan, đó là giai đoạn ban đầu được đặc trưng bởi quá trình chết và apoptosis và hoại tử tế bào lan rộng Đặc trưng bởi giai đoạn sau.
B. Viêm gan mãn tính và bệnh gan mãn tính: CD95L có thể được phát hiện trong các tế bào lympho thâm nhập vào gan của hầu hết các bệnh nhân bị viêm gan mãn tính, và các tế bào lympho biểu hiện CD95L có thể là tế bào tác động chính để bắt đầu quá trình apoptosis của tế bào gan.
Biểu hiện CD95L và CD95, tổn thương DNA và quá trình apoptosis là đáng kể nhất trong vùng viêm giao diện, phù hợp với quá trình nhiễm virus trong gan; một số lượng lớn CTL xâm nhập cục bộ biểu hiện CD95L và CD95 làm trung gian cho quá trình apoptosis của tế bào gan, là sự khác biệt giữa viêm gan virus
Đối với các đặc điểm khác của tổn thương gan. Trong bệnh viêm gan siêu vi, tế bào gan cũng biểu hiện CD95 và CD95L cùng một lúc, và chúng không chỉ là tế bào đích mà còn là tế bào hiệu ứng trong quá trình apoptosis.
Mức độ biểu hiện CD95L và CD95 trong tế bào gan phù hợp với hoạt động của các tổn thương viêm. Mô gan bình thường là âm tính.
CH nhẹ (viêm gan mạn tính) có thể không có hoặc biểu hiện yếu, chỉ có một số tế bào dương tính hiện diện ở vùng viêm giao diện; CH vừa và nặng thường biểu hiện ở mức độ trung bình và mạnh, có nhiều tế bào dương tính ở vùng viêm giao diện, ngoài ra còn có rải rác và rải rác trong các tiểu thùy gan. Phân bố khuếch tán đều.
CH kết hợp với LC sớm và LC hoạt động thường có tình trạng viêm nặng, và CD95L và CD95 thường được biểu hiện ở cường độ trung bình đến cường độ; trong khi biểu hiện của HCC yếu và giảm apoptosis là cơ chế hình thành khối u.
(3) Đột biến do vi rút:
Sau khi cơ thể con người bị nhiễm vi rút đột biến hoặc nhiễm vi rút hoang dại, phản ứng miễn dịch gây ra là khác nhau.
Ý nghĩa sinh học của vi rút đột biến có thể bao gồm: trốn tránh khả năng miễn dịch tự nhiên hoặc do vắc xin tạo ra, gây ra kháng thuốc, thay đổi cơ chế gây bệnh và thậm chí thay đổi chế độ sinh sản của các loài và mô.
Do đó, sự đột biến của virus có thể là một yếu tố quan trọng trong việc lây truyền virus, khả năng gây bệnh và kết quả.
Vùng tiền C tạo thành cấu trúc kẹp tóc (tín hiệu đóng gói – cấu trúc vòng gốc), cần thiết để đóng gói RNA tiền bộ gen, và có thể giải thích sự phổ biến cực kỳ cao của đột biến TAG tại codon 28. G1896 và T1858 là cặp bazơ không bền của cấu trúc vòng gốc epsilon nói trên, đột biến G chuyển ntl896 thành A làm cho cấu trúc vòng gốc ổn định hơn.
Do đó, đột biến tiền C / A83 có thể là một hiện tượng phổ biến trong lịch sử nhiễm HBV tự nhiên, và nó chủ yếu xảy ra trong quá trình chuyển đổi huyết thanh HBe và thường chỉ ra sự thuyên giảm của bệnh.
Sự phân bố các biến dị gen C không ngẫu nhiên, hầu hết tập trung ở 3 chuỗi ngắn 13, 18 và 9 axit amin AA48-60, AA84-101 và AAl47-155, có tỷ lệ thay thế cao hơn các bộ phận khác.
Vùng biểu hiện gen C là mục tiêu chính của phản ứng miễn dịch của vật chủ, có liên quan đến sự xuất hiện của bệnh tật và sự thanh thải của các tế bào gan bị nhiễm bệnh.
Sự đột biến của vùng gen C có thể là một chiến lược được HBV sử dụng để tránh sự thanh thải miễn dịch trong quá trình lây nhiễm mãn tính của nó, để quá trình lây nhiễm tiếp tục và bệnh trầm trọng hơn.
Đột biến của gen khởi động (cp) C cũng làm cho HBcAg bị thiếu. Người ta nhận thấy rằng A → T của ntl762 và G → A của ntl764 có liên quan đến kiểu hình HBeAg (-) và viêm gan nặng cấp tính.
Vùng cp nằm trong ntl643-1849, cấu trúc và chức năng của nó phức tạp hơn. Nó trùng lặp một phần với vùng tiền C của gen X và gen C; DR1 và chất tăng cường II nằm trong vùng của nó; tiền CmRNA và tiền bộ gen C / PmRNA đều bắt đầu ở đây .
cp được cấu tạo bởi hai phần: trình tự điều hòa ngược dòng lõi (CURS) và trình tự khởi động lõi cơ bản (Bcp). Bcp là 108 nucleotide trong đoạn n1744-1849. Vùng DR1 chứa và vùng bắt đầu của hai mRNA rất Việc bảo tồn cho thấy rằng sự ổn định của các vùng này là cần thiết cho sự nhân lên của virus.
Chỉ bị nhiễm các chủng biến thể cp vẫn có thể có hiệu giá HBV DNA cao, có thể so sánh với các chủng bị nhiễm các chủng hoang dã, cho thấy rằng các biến thể này không ảnh hưởng đáng kể đến sự phiên mã của tiền gen HBV.
cp không đồng nhất và có thể không có những thay đổi cụ thể liên quan đến tình trạng HBe hoặc viêm gan nặng cấp tính. Sự thay thế của ntl762 và ntl764 đôi khi được thấy trong viêm gan nặng cấp tính, viêm gan mãn tính và các bệnh gan mãn tính khác, và có thể không phải là kiểu hình HBeAg.
Ba, sáu con đường lây truyền chính của bệnh viêm gan B
(1) Truyền máu hoặc sản phẩm máu: chẳng hạn như truyền máu toàn phần, huyết tương, huyết thanh hoặc các sản phẩm máu khác, truyền qua đường tiêm chích qua đường máu.
Các sản phẩm máu bị nhiễm virus viêm gan B như albumin, tiểu cầu hoặc máu truyền cho người nhận hầu hết sẽ gây ra viêm gan sau truyền máu, ngoài ra virus viêm gan B cũng có thể bị nhiễm trong quá trình chạy thận nhân tạo và lọc thận.
(2) Lây truyền qua thai nhi (Ba dương tính nhỏ lây truyền): Ví dụ, phụ nữ mang thai mang vi rút sang trẻ sơ sinh qua đường lây truyền dọc ống sinh; phụ nữ mang thai bị viêm gan khi mang thai sẽ lây sang thai nhi.
Có khoảng 140 triệu người dương tính với HBSAg ở Trung Quốc, và 85% trong số đó lây truyền qua đường lây truyền từ mẹ sang con. Lây truyền dọc là một lý do quan trọng cho sự lây lan và thường xuyên của bệnh viêm gan B ở Trung Quốc .
Cũng có một số ít những người giao tiếp giữa cha và con bị bệnh viêm gan B. Phần lớn đường lây truyền của mẹ và con là qua ống sinh hoặc nhiễm trùng trong tử cung.
(3) Lây truyền vô tính: Nếu dụng cụ y tế bị nhiễm vi rút viêm gan B và không được khử trùng kỹ lưỡng hoặc xử lý đúng cách, nó có thể gây ra sự lây truyền;
Sử dụng bơm tiêm để ngăn ngừa việc tiêm chích cho một số đối tượng đã được chủng ngừa cũng là một trong những cách lây truyền vi rút viêm gan B; qua đường máu Bệnh nhân lây truyền thường là mục tiêu lây truyền bệnh viêm gan B.
(4) Lây truyền qua đường tình dục: Trong những năm gần đây, các báo cáo nước ngoài về quan hệ tình dục bừa bãi, đồng tính và dị tính đã khẳng định rằng việc lây truyền viêm gan B
Đường tình dục là một con đường quan trọng để lây nhiễm cho bạn tình, và sự lây truyền này cũng bao gồm cả việc lây truyền giữa các cặp vợ chồng trong gia đình.
(5) Sự lây truyền của côn trùng đốt: muỗi và các loài côn trùng hút máu khác nhau ở vùng nhiệt đới và cận nhiệt đới có thể đóng một vai trò trong việc truyền bệnh viêm gan B.
(6) Lây truyền qua tiếp xúc gần gũi trong cuộc sống: Tiếp xúc gần gũi lâu dài với bệnh nhân hoặc người mang vi rút viêm gan B, nước bọt, nước tiểu, máu, mật, sữa có thể làm ô nhiễm thiết bị và đồ vật để lây bệnh viêm gan B.
Chủ yếu đề cập đến quan hệ tình dục, tiếp xúc gần gũi trong cuộc sống hàng ngày (như sử dụng bàn chải đánh răng, khăn tắm, tách trà và bộ đồ ăn), tất cả đều có thể bị nhiễm virus viêm gan B.
Virus viêm gan B có thể xâm nhập vào cơ thể của những người tiếp xúc gần qua niêm mạc bị tổn thương.
Các triệu chứng thường gặp bệnh viêm gan B : tăng transaminase, sụt cân, mệt mỏi, buồn nôn, chán ăn, gan to, giảm sức đề kháng, sốt, bơ phờ.
Thời gian ủ bệnh của bệnh viêm gan B là 6 tuần đến 6 tháng, thông thường là 3 tháng. Thời kỳ từ khi virus viêm gan xâm nhập đến khi có các triệu chứng lâm sàng đầu tiên được gọi là thời kỳ ủ bệnh. Thời gian ủ bệnh thay đổi theo loại, số lượng, độc lực và tình trạng miễn dịch của mầm bệnh.
Người bệnh viêm gan B thường xuyên cảm thấy mệt mỏi , uể oải, sốt nhẹ . Mất ngủ , hay mơ, … có thể liên quan đến điều này.
Trong bệnh viêm gan B, chức năng gan không bình thường, giảm tiết mật, chán ăn, buồn nôn , váng đầu , khó chịu vùng bụng trên, chướng bụng ….
Khi bệnh viêm gan B nặng, chức năng gan bị suy giảm, việc hấp thu, kết hợp, bài tiết và bài tiết bilirubin bị cản trở, nồng độ bilirubin trong máu tăng cao. Bilirubin được bài tiết qua nước tiểu và màu nước tiểu chuyển sang màu vàng, đây là biểu hiện sớm nhất của bệnh vàng da.
Nồng độ bilirubin trong máu tiếp tục tăng, có thể khiến mắt và da bị vàng. Do sự bài tiết của acid mật bị cản trở, nồng độ acid mật trong máu tăng cao, acid mật lắng đọng quá mức trên da gây kích thích dây thần kinh ngoại biên, có thể gây ngứa da .
Bệnh viêm gan B mãn tính thường không gây đau dữ dội. Một số bệnh nhân có thể có cảm giác khó chịu, đau âm ỉ, đau nhói hoặc đau như gõ ở vùng bụng trên bên phải và xương sườn phải.
Nếu đau dữ dội vùng gan cần chú ý khả năng mắc bệnh đường mật, ung thư gan, bệnh đường tiêu hóa để tránh chẩn đoán nhầm.
Bệnh nhân bệnh viêm gan B thường bị to gan do viêm, xung huyết , phù nề, ứ mật. Ở giai đoạn muộn, một số lượng lớn tế bào gan bị phá hủy, các mô xơ teo lại, gan có thể bị teo nhỏ lại.
Trong giai đoạn đầu của bệnh viêm gan B cấp tính hoặc viêm gan mãn tính , lá lách không to rõ ràng, khi tăng áp lực tĩnh mạch cửa có thể làm xung huyết lá lách gây ra hiện tượng lách to.
bệnh viêm gan B mãn tính, đặc biệt là những người bị xơ gan, da có màu sẫm và xỉn màu, được gọi là bệnh gan. Lòng bàn tay lớn và lòng bàn tay nhỏ bị tắc nghẽn đáng kể.
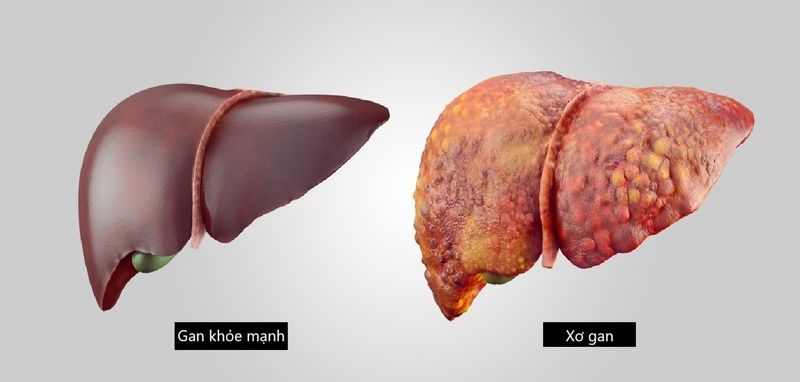

Mở rộng Radial của cụm da có hình dạng như một nhóm nhện mao mạch, cho biết nhện nevi , các bộ phận khác cũng có thể xảy ra.
Nam giới bệnh viêm gan B có thể bị rối loạn cương dương, tăng sản vú đối xứng hoặc không đối xứng, sưng và đau và phát triển vú, và đôi khi có thể bị chẩn đoán nhầm là ung thư vú;
Phụ nữ bệnh viêm gan B có thể bị rối loạn kinh nguyệt, vô kinh và giảm ham muốn tình dục. Điều này có thể liên quan đến việc giảm chức năng gan, giảm sự bất hoạt của estrogen và tăng estrogen trong cơ thể.
bệnh viêm gan B mãn tính lâu ngày không lành, hay tái phát, mô liên kết xơ trong gan tăng sinh, hoạt tính suy thoái của nó tương đối hoặc hoàn toàn không đủ, một lượng lớn chất nền ngoại bào được lắng đọng tạo thành xơ gan.
Nếu gan bị xơ hóa kèm theo phá hủy cấu trúc tiểu thùy gan (nốt tái tạo gan) thì được gọi là xơ gan. Về mặt lâm sàng, khó có thể tách biệt hoàn toàn cả hai Bệnh gan mãn tính là một quá trình phát triển liên tục từ gan bị xơ hóa đến xơ gan.
(1) Viêm gan ruột cấp: Theo diễn biến bệnh có thể chia làm 3 giai đoạn, tổng thời gian điều trị từ 2 đến 4 tháng. Tiền vàng da: Khởi phát tương đối chậm, chủ yếu là các triệu chứng tiêu hóa như chán ăn, buồn nôn, mệt mỏi.
Một số ít có các triệu chứng bệnh viêm gan B về đường hô hấp, thỉnh thoảng sốt cao, đau bụng dữ dội và một số ít có biểu hiện giống bệnh huyết thanh. Giai đoạn này kéo dài vài ngày đến 2 tuần, và giai đoạn vàng da: củng mạc và vàng da rõ rệt, đạt đến đỉnh điểm trong vài ngày đến 2 tuần.
Sau khi bắt đầu vàng da, sốt giảm dần, cảm giác thèm ăn được cải thiện, một số bệnh nhân bệnh viêm gan B vẫn còn các triệu chứng tiêu hóa trong thời gian ngắn. Gan to và mềm, có cảm giác đau và mềm.
Khoảng 5% đến 10% bệnh nhân bệnh viêm gan B có lách to. Các tế bào bạch cầu ngoại vi nói chung bình thường hoặc hơi thấp, và ALT (alanin aminotransferase huyết thanh) tăng cao đáng kể, và giai đoạn này kéo dài từ 2 đến 6 tuần.
Thời kỳ hồi phục bệnh viêm gan B: Vàng da giảm dần, các triệu chứng khác nhau dần biến mất, gan và lá lách co lại bình thường, chức năng gan trở lại bình thường. Thời kỳ này kéo dài khoảng 4 tuần.
(2) bệnh viêm gan B không do ruột cấp: Khởi phát chậm, các triệu chứng tương tự như các biểu hiện tiền vàng da nêu trên, nhiều bệnh nhân không có triệu chứng rõ ràng.
Trong quá trình khảo sát tổng quát hoặc xét nghiệm máu bệnh viêm gan B, đôi khi thấy ALT huyết thanh tăng cao, bệnh nhân dần hồi phục sau hơn 3 tháng. Khoảng 5% đến 10% trở thành viêm gan mãn tính.

2. Diễn biến của bệnh viêm gan B mãn tính kéo dài hơn nửa năm, thời gian khởi phát cũng có thể ẩn đi, khi khám sức khỏe thường phát hiện ra. Các triệu chứng rất đa dạng, tái phát hoặc kéo dài.
Các triệu chứng rối loạn tiêu hóa thường gặp hơn, biểu hiện là chán ăn, ngấy dầu, buồn nôn, chướng bụng, đi ngoài phân lỏng… Hầu hết bệnh nhân có biểu hiện mệt mỏi và khó chịu ở gan.
Các triệu chứng thường nặng hơn khi mệt mỏi, thay đổi tâm trạng và thay đổi khí hậu. Một số bệnh nhân bị sốt nhẹ và rối loạn thần kinh, chẳng hạn như chóng mặt, mất ngủ, mơ hoặc hôn mê, không chú ý, giảm trí nhớ, cáu kỉnh, khó chịu chung, đau thắt lưng và chân, v.v.
Một số bệnh nhân có thể có xu hướng chảy máu , biểu hiện là chảy máu lợi, chảy máu mũi, xuất huyết điểm dưới da hoặc bầm máu. Một số ít bệnh nhân không có triệu chứng. Bệnh nhân bị viêm gan mãn tính trung bình và nặng có tình trạng sức khỏe suy giảm, có biểu hiện bệnh gan, da xỉn màu và xám xám.
Có thể thấy gan bàn tay, hình mạng nhện, gan và lá lách to ra, kết cấu trung bình hoặc cứng, sờ và gõ đau, và lách to dần. Một số bệnh nhân bị rối loạn nội tiết như rậm lông, mụn trứng cá, teo tinh hoàn, nữ hóa tuyến vú, sắc tố núm vú, nổi cục ở vú.
Kiểm tra trong phòng thí nghiệm cho thấy ALT và bilirubin tăng nhiều lần hoặc liên tục, AST (aspartate aminotransferase) thường tăng, một số bệnh nhân r-glutamyl transpeptidase, arginine succinate lyase (ASAL), Alkaline phosphatase cũng tăng cao.
Cholinesterase và cholesterol giảm đáng kể thường cho thấy gan bị tổn thương nặng. Xét nghiệm giữ màu xanh chàm và xác định axit mật trong huyết thanh 2 giờ sau bữa ăn có thể phản ánh bệnh gan một cách nhạy cảm hơn.
Ở những bệnh nhân bị viêm gan mãn tính từ trung bình đến nặng, albumin (A) giảm, globulin (G) tăng, tỷ lệ A / G đảo ngược, đồng thời gamma globulin và IgG cũng tăng.
Prothrombin có thời gian bán hủy ngắn và có thể phản ánh kịp thời mức độ nghiêm trọng của tổn thương gan, các yếu tố đông máu V và VII thường bị giảm.
Một số bệnh nhân có thể có các tự kháng thể, chẳng hạn như kháng thể chống nhân, kháng thể chống cơ trơn, kháng thể chống ty thể, yếu tố dạng thấp và tế bào lupus.
Các biểu hiện của hệ thống ngoài gan có thể xảy ra trong bất kỳ giai đoạn nào của bệnh viêm gan virus , và viêm gan mãn tính thường gặp hơn. Hệ tiêu hóa có thể bị viêm túi mật, viêm đường mật, viêm dạ dày, viêm tụy, v.v …
Hệ hô hấp có thể bị viêm màng phổi, viêm phổi; thận có thể bị viêm cầu thận, nhiễm toan ống thận, v.v … hệ tuần hoàn có thể bị viêm đa mạch, viêm cơ tim. , Viêm màng ngoài tim, v.v …;
Hệ thống máu có thể có ban xuất huyết giảm tiểu cầu, mất bạch cầu hạt, thiếu máu bất sản và thiếu máu tán huyết, v.v …; da có thể nổi mụn trứng cá, viêm da sẩn ở trẻ sơ sinh (bệnh Gianotti), ban xuất huyết dị ứng, ban đỏ hình bướm ở mặt
Hệ thần kinh có thể bị viêm màng não, viêm tủy, viêm đa dây thần kinh, hội chứng Guillain-Barré, v.v …; cũng có thể bị viêm khớp, đau khớp và các bệnh khác. Sự xuất hiện của các biểu hiện hệ thống ngoài gan trong viêm gan virus có liên quan đến các yếu tố sau:
① Sự xâm nhập của virus và phản ứng của cơ thể đối với sự nhiễm virus.
②Sự hình thành và lắng đọng các phức hợp miễn dịch.
③Lesion do phản ứng miễn dịch tế bào của cơ thể gây ra.
④ Ảnh hưởng thứ phát sau tổn thương nhu mô gan.
(1) Viêm gan nặng cấp tính: còn được gọi là viêm gan tối cấp. Lúc đầu giống như viêm gan vàng da cấp tính, nhưng tình trạng bệnh tiến triển nhanh chóng.
Các triệu chứng tâm thần xuất hiện trong vòng 10 ngày kể từ khi khởi phát, chẳng hạn như hưng phấn, tính cách và hành vi bất thường, câu hỏi không được trả lời, ngày đêm sai, đi lại không ổn định, mờ mắt và hôn mê.
Vàng da đậm dần, độ mờ da gáy nhanh chóng, có các phản xạ run như vẩy nến và bệnh lý. Xu hướng chảy máu rõ ràng, hạ đường huyết, sốt cao và cổ trướng xuất hiện trong suốt quá trình của bệnh .
Khả năng bị phù não cao, một số bệnh nhân bị bệnh não. Ở giai đoạn muộn xảy ra hạ huyết áp khó chữa và suy thận cấp. Tổng số lượng bạch cầu trong máu ngoại vi của bệnh nhân tăng lên, và bilirubin huyết thanh> 171μmol / L, hoặc tăng nhanh trung bình hàng ngày là 17,1 ~ 34,2μmol / L.
Phân ly vàng da do men xảy ra ở hầu hết các bệnh nhân. Tình trạng rất nguy kịch và tiên lượng rất xấu, diễn biến của bệnh thường không quá 3 tuần.
(2) Viêm gan nặng bán cấp: hay còn gọi là viêm gan nặng bán cấp. Khởi phát thường giống với viêm gan vàng da cấp tính. Các triệu chứng nghiêm trọng hơn, bệnh nhân vô cùng yếu, rõ ràng là chán ăn, buồn nôn và nôn thường xuyên, chướng bụng không thể chịu được và cổ trướng.
Gan giảm dần, vàng da tăng nhanh, bilirubin huyết thanh lớn hơn 171μmol / L, xu hướng xuất huyết rõ ràng, thời gian prothrombin kéo dài và hoạt tính dưới 40%. Protein huyết thanh giảm, tỷ lệ A / G ngược, ALT tăng ở giai đoạn đầu, sau đó là hiện tượng vàng da phân ly, tỷ lệ AST / ALT> 1.
Bệnh não gan thường xảy ra ở giai đoạn muộn của bệnh, giai đoạn sau có thể xảy ra chảy máu nặng, mất cân bằng điện giải, hội chứng gan-thận, nhiễm trùng nặng và suy đa tạng.
Diễn biến của bệnh kéo dài, có thể đến vài tháng. Một số bệnh nhân có thể hồi phục, nhưng thường phát triển thành xơ gan sau khi hoại tử.
(3) Viêm gan nặng mãn tính: Biểu hiện lâm sàng giống viêm gan nặng bán cấp. Tuy nhiên, đó là trên cơ sở tình trạng mang vi rút viêm gan mãn tính, xơ gan hoặc viêm gan B, gan đã bị tổn thương nặng.
Viêm gan mãn tính có thể xảy ra lặp đi lặp lại và dần dần xấu đi trở thành viêm gan nặng mãn tính, hoặc khởi phát giống như viêm gan nặng cấp tính hoặc bán cấp tính và chẩn đoán được xác nhận bằng khám nghiệm tử thi sau khi chết.
Các biểu hiện chính là vàng da tăng dần, suy giảm hoạt động prothrombin tiến triển, xuất hiện một lượng lớn dịch cổ trướng khó giải quyết, nhiễm trùng nặng lặp đi lặp lại và rối loạn điện giải khó điều chỉnh.
Bệnh nhân loại này thường bị giảm oxy máu và rối loạn thông khí. Trong những năm gần đây, do tăng cường điều trị, hơn một nửa số bệnh nhân không phát bệnh não gan, hoặc chỉ xuất hiện trước giai đoạn cuối đời, thường tử vong do xuất huyết tiêu hóa trên, hội chứng gan thận, nhiễm trùng nặng.
4. Viêm gan ứ mật Viêm gan ứ mật cấp tính khởi phát tương tự như viêm gan vàng da cấp tính, nhưng triệu chứng nhẹ, vàng da nặng dần và kéo dài trên 3 tuần, da bệnh nhân ngứa, màu phân nhạt hơn và có thể xám trong thời gian ngắn.
Gan to, bilirubin huyết thanh tăng lên rõ rệt, chủ yếu là bilirubin trực tiếp. R-glutamyl transpeptidase, phosphatase kiềm, cholesterol và acid mật huyết thanh đều tăng.
Khi bắt đầu bệnh, ALT tăng nhiều, nhưng nhanh chóng giảm, và xuất hiện hiện tượng vàng da phân ly do enzym. Hoạt động prothrombin của một số bệnh nhân giảm khi họ nhập viện, nhưng sau khi bổ sung vitamin K1, họ nhanh chóng được điều chỉnh sau 3 đến 7 ngày. Không có biểu hiện của tắc nghẽn ngoài gan bằng siêu âm B.
Các hạng mục giám định: năm hạng mục về bệnh viêm gan B, chức năng gan, siêu âm gan và túi mật, xét nghiệm máu, DNA viêm gan B
Ở những bệnh nhân cấp tính vàng da bệnh viêm gan, bilirubin nước tiểu và urobilinogen dương tính trước khi vàng da xuất hiện.
(1) Hình ảnh máu:
Tổng số lượng bạch cầu thấp hơn một chút so với mức bình thường, số lượng bạch cầu trung tính khác biệt có thể giảm, và tương đối tăng tế bào lympho.
(2) Bilirubin huyết thanh:
Bilirubin huyết thanh trong thời kỳ vàng da tăng, theo xu hướng tăng hàng ngày và thường đạt đỉnh trong vòng 1 đến 2 tuần.
(3) Xác định enzym huyết thanh:
Vàng da bắt đầu tăng dần trước khi xuất hiện và đạt đến đỉnh điểm ở giai đoạn cực đoan. Viêm gan cấp tính có thể có hoạt tính enzym cực cao và giai đoạn phục hồi giảm dần theo bilirubin huyết thanh.
Trong bệnh viêm gan mãn tính , ALT có thể dao động lặp lại nhiều lần. Trong trường hợp viêm gan nặng, ALT giảm khi bilirubin tăng mạnh, đây được gọi là “phân tách vàng da do enzym”, có nghĩa là bệnh nghiêm trọng.
Phần lớn AST (khoảng 4/5) tồn tại trong ty thể tế bào (ASTm), và phần còn lại nằm trong dịch tế bào (ASTs). Khi ty thể bị tổn thương, AST huyết thanh sẽ tăng lên đáng kể, phản ánh mức độ nghiêm trọng của tổn thương tế bào gan.
Vi rút, đặc biệt là phương án STD cấp tính , giá trị ALT AST cao hơn giá trị này. Tỷ lệ ALT / AST gần bằng 1 khi bệnh viêm gan virus mạn tính hoạt động liên tục, AST thường cao hơn ALT khi xơ gan.
Ngoài sự gia tăng ALT và AST trong thời kỳ hoạt động của bệnh viêm gan siêu vi, nó cũng sẽ gia tăng trong các bệnh gan khác (như ung thư gan, nhiễm độc, tổn thương gan do thuốc hoặc rượu, v.v., các bệnh về mật, viêm tụy, bệnh cơ tim, suy tim, v.v.) , Nên chú ý đến giấy tờ tùy thân.
Những thành phần này có thể thay đổi trong tổn thương gan cấp tính và mãn tính, nhưng độ nhạy và phạm vi thay đổi thấp hơn nhiều so với transaminase. Nghiện rượu cũng có thể làm tăng r-GT.
Trong viêm gan mạn tính, sau khi bệnh đường mật khỏi, r-GT tăng chứng tỏ bệnh vẫn còn hoạt động, khi suy gan, các microsome tế bào gan bị tổn thương nặng, tổng hợp r-GT giảm, r-GT máu cũng giảm theo.
Nó có thể tăng lên đáng kể trong tắc nghẽn ống mật trong gan và các tổn thương chiếm không gian gan. r-GT có thể làm tăng ứ mật và tổn thương tế bào gan, và nó có thể được sử dụng để xác định liệu sự gia tăng ALP có liên quan đến bệnh gan mật hay không.
(4) Kiểm tra chức năng chuyển hóa protein bệnh viêm gan B:
Hạ kali máu và tăng globulin huyết là các chỉ số huyết thanh học đặc trưng để chẩn đoán xơ gan. Hạ albumin máu là một chỉ số quan trọng của bệnh gan, và mức độ giảm của nó phụ thuộc vào mức độ nghiêm trọng và giai đoạn của bệnh gan .
Pre-Alb trong huyết thanh bệnh viêm gan B có thời gian bán hủy chỉ 1,9 ngày nên nhạy cảm hơn với những thay đổi của tổn thương nhu mô gan, mức giảm phù hợp với mức độ tổn thương của tế bào gan, cơ chế thay đổi của nó cũng tương tự như Alb.
Trong cấp tính viêm gan virus, viêm gan mãn tính và xơ gan (hoạt động), có thể có thấp và trung bình ngắn hạn tăng lên. Sự gia tăng các dấu AFP sự tái sinh của tế bào gan .
Ở những bệnh nhân bệnh viêm gan B với rộng hoại tử tế bào gan , tăng AFP có thể có một tiên lượng tốt hơn. Bệnh nhân có nồng độ AFP huyết thanh cực cao, và rất có thể mắc ung thư biểu mô tế bào gan.
Trong bệnh viêm gan B nặng và suy gan, amoniac không thể tổng hợp thành urê để bài tiết; amoniac trong máu có thể tăng ở bệnh nhân xơ gan và tuần hoàn bàng hệ.
Amoniac ức chế lưu lượng máu não, chuyển hóa glucose và cung cấp năng lượng, tác động trực tiếp lên màng tế bào thần kinh. Ngộ độc amoniac là một trong những nguyên nhân chính gây hôn mê gan , nhưng nồng độ amoniac trong máu có thể không phù hợp với sự xuất hiện và mức độ nghiêm trọng của bệnh viêm gan B.
Phân tích hồ sơ axit amin trong huyết tương có ý nghĩa lớn đối với việc chẩn đoán và tiên lượng bệnh não gan . Các axit amin chuỗi nhánh của bệnh nhân viêm gan nặng và xơ gan gần như bình thường hoặc giảm, axit amin thơm tăng lên đáng kể, dẫn đến giảm tỷ lệ nhánh / thơm (bình thường 3,0 ~ 3,5) ,
Nó thậm chí có thể lộn ngược trong bệnh não gan.
(5) Thời gian prothrombin (PT) và hoạt động (PTA):
Mức độ kéo dài của PT cho biết mức độ hoại tử tế bào gan và suy gan . Do giảm tổng hợp các yếu tố đông máu liên quan trong bệnh gan nên có thể gây kéo dài PT, và thời gian bán thải của các yếu tố đông máu liên quan rất ngắn, như Ⅶ (4 ~ 6h), Ⅹ ( 48 ~ 60h), Ⅱ (72 ~ 96h)
Vì vậy nó có thể phản ánh suy gan nhanh hơn. PTA của viêm gan nặng hầu hết là dưới 40%, và PTA giảm xuống dưới 20%, thường cho thấy tiên lượng xấu.
Lưu ý: Kéo dài PT cũng có thể gặp ở những bệnh nhân thiếu hụt yếu tố đông máu bẩm sinh, đông máu lan tỏa nội mạch , thiếu vitamin K và cần được phân biệt.
(6) Các xét nghiệm liên quan đến chuyển hóa lipid bệnh viêm gan B
Cholesterol toàn phần (TC) huyết thanh giảm đáng kể trong viêm gan nặng, có người cho rằng tiên lượng xấu khi TC <2,6mmol / L. TC có thể tăng đáng kể trong viêm gan ứ mật và tắc nghẽn ngoài gan.
Triacylglycerol (TG) huyết thanh có thể làm tăng tổn thương tế bào gan và vàng da tắc nghẽn bên trong và bên ngoài gan.
(7) Chẩn đoán xơ hóa gan:
Trong bệnh gan mãn tính, sự hình thành chất nền ngoại bào (ECM) và sự suy thoái của chất nền bị mất cân bằng, dẫn đến lắng đọng quá nhiều ECM và xơ hóa.
Việc phát hiện các thành phần nền, các sản phẩm phân hủy của nó và các enzym tham gia vào quá trình chuyển hóa trong huyết thanh có thể được sử dụng làm dấu hiệu huyết thanh để chẩn đoán xơ hóa gan.
3. Phát hiện các dấu hiệu vi rút HBV bệnh viêm gan B
(1) HBsAg và anti-HBs:
HBsAg bệnh viêm gan B dương tính là một trong những dấu hiệu của nhiễm HBV, và nó không phản ánh sự nhân lên, lây nhiễm và tiên lượng của virus. HBsAg là một kháng nguyên xuất hiện sớm hơn trong trường hợp nhiễm HBV cấp tính, và nó thường kéo dài từ 2 đến 6 tháng để trở thành âm tính.
HBsAg bệnh viêm gan B có thể được phát hiện trong huyết thanh từ 2 đến 8 tuần trước khi tăng transaminase huyết thanh của người nhiễm HBV. Viêm gan mãn tính, xơ gan do viêm gan và người mang HBsAg có thể cho thấy phản ứng dương tính trong huyết thanh và kéo dài hơn nửa năm.
Anti-HBs phản ánh khả năng miễn dịch bảo vệ của cơ thể đối với HBV. Nó xuất hiện trong giai đoạn phục hồi của nhiễm HBV hoặc sau khi tiêm phòng viêm gan B. Đây là một kháng thể trung hòa.
Hiệu lực của anti-HBs song song với khả năng bảo vệ, khi hiệu giá thấp hơn 10.000 U / L, nó không thể ngăn ngừa sự tái nhiễm HBV. Một số ít bệnh nhân phát triển các phức hợp miễn dịch được hình thành bởi anti-HBs và HBsAg ngay sau khi nhiễm trùng, gây phát ban da, viêm khớp , viêm thận, v.v.
Ở những bệnh nhân bệnh viêm gan B có HBsAg dương tính, có thể không phát hiện thấy anti-HBs trong huyết thanh. Người mang HBV mạn tính khó sản sinh ra anti-HBs vì khả năng dung nạp miễn dịch và khả năng hình thành kháng thể của tế bào B bị khiếm khuyết.
Viêm gan nặng có thể tạo ra nồng độ anti-HBs cao vì phản ứng miễn dịch của cơ thể rất hoạt động. Ngoài ra, phân tích peptide tổng hợp đã xác nhận rằng HBV pre-S1 là phối tử hấp phụ vào các tế bào đích, và pre-S2 đóng vai trò hỗ trợ trong quá trình hấp phụ.
Sự hấp phụ của HBV vào tế bào đơn nhân máu ngoại vi chủ yếu liên quan đến tiền S2. Các kháng thể pre-S1 và pre-S2 được thấy trong giai đoạn cấp tính và giai đoạn đầu hồi phục của viêm gan B, chứng tỏ virus đang hoặc đã được loại bỏ và tiên lượng tốt.
Không thể tìm thấy kháng thể tiền bệnh viêm gan B S trong huyết thanh của người mang HBsAg và bệnh nhân viêm gan B mãn tính, và sự chậm trễ xuất hiện của kháng thể tiền S có nghĩa là tiên lượng xấu.
Ý nghĩa lâm sàng chính của pre-S1 và pre-S2 là: chỉ điểm cho sự nhân lên của virus; một trong những chỉ số tham chiếu để đánh giá hiệu quả của thuốc.
(2) HBeAg và anti-HBe:
HBeAg trong huyết thanh dương tính ở bệnh nhân bệnh viêm gan B cấp tính và mãn tính và những người mang mầm bệnh không có triệu chứng.
Cần lưu ý: HBeAg và HBVDNA, có liên quan mật thiết đến hoạt động của DNA polymerase và các hạt Dane, là dấu hiệu bệnh toxemia , cho thấy bệnh nhân đang lây nhiễm.
Từ giai đoạn đầu của thời kỳ ủ bệnh nhiễm HBV đến khi bắt đầu có các triệu chứng lâm sàng trong 10 tuần, có thể phát hiện ra bệnh trong huyết thanh. Sau đó suy yếu dần dần biến mất. 3 đến 4 tháng sau khi khởi phát bệnh viêm gan B cấp, HbeAg chuyển sang âm tính, cho thấy tiên lượng tốt.
HBeAg tiếp tục dương tính cho thấy tình trạng viêm gan đang phát triển mãn tính.
Anti-HBe xuất hiện sau khi HBeAg biến mất, anti-HBe dương tính cho thấy khả năng lây nhiễm bị suy yếu hoặc biến mất, nhưng ở một số bệnh nhân hoặc người mang virus viêm gan B mãn tính, mặc dù anti-HBe dương tính, HBVDNA vẫn có thể được phát hiện trong tuần hoàn máu, chứng tỏ anti-HBe dương tính.
bệnh viêm gan B không nhất thiết là không lây nhiễm. Tỷ lệ phát hiện anti-HBe ở những bệnh nhân viêm gan mãn tính, xơ gan và ung thư gan tăng liên tiếp, cho thấy rằng anti-HBe dương tính không nhất thiết có tiên lượng tốt.
(3) HBcAg và anti-HBc:
HBcAg là thành phần cốt lõi của HBV và chứa axit nucleic của virus. Khi HBcAg dương tính, có nghĩa là virus đã nhân lên và có khả năng lây nhiễm.
Vì HBcAg được bao bọc xung quanh HBsAg trong vòng tuần hoàn, và một lượng nhỏ HBcAg tự do có thể chuyển hóa thành HBeAg hoặc kết hợp với anti-HBc để tạo thành một phức hợp miễn dịch
HBcAg không thể được phát hiện từ huyết thanh của bệnh nhân bằng các phương pháp chung mà chỉ phát hiện được trong tế bào gan. .
Với sự cải tiến của công nghệ phát hiện, khi các hạt Dane được xử lý bằng chất tẩy rửa, HBcAg có thể được giải phóng. Hiệu giá HBsAg cao, HBeAg và DNA polymerase dương tính, HBcAg hầu hết là dương tính.
Anti-HBc là tổng số kháng thể của kháng nguyên lõi virus viêm gan B. Loại kháng thể đầu tiên xuất hiện sau khi nhiễm HBV là kháng thể lõi loại IgM (anti-HBcIgM).
Giá trị anti-HBcIgM cao là một dấu hiệu quan trọng của nhiễm HBV cấp tính hoặc gần đây và nó hoạt động trong bệnh viêm gan mãn tính. Thời kỳ cũng thường tích cực. Kháng thể lõi không phải là kháng thể trung hòa.
Anti-HBcIgG có thể tồn tại trong nhiều năm và là dấu hiệu chỉ điểm cho việc nhiễm bệnh viêm gan B HBV trước đó. Việc phát hiện anti-HBc có thể làm tăng tỷ lệ phát hiện nhiễm HBV, giúp ích cho việc chẩn đoán và điều tra dịch tễ học.
(4) HBVDNA và DNA polymerase:
Việc xác định DNA polymerase có thể phản ánh một cách nhạy cảm hơn hiệu quả của thuốc kháng vi-rút. Công nghệ lai axit nucleic có thể phát hiện trực tiếp DNA của HBV, nếu HBsAg và HBeAg âm tính nhưng HBVDNA dương tính có nghĩa là HBV đang nhân lên và bệnh nhân đang lây nhiễm.
DNA polymerase hoạt động như một enzyme sao chép ngược trong quá trình sao chép của virus. Hoạt tính của nó càng cao thì hoạt động sao chép của virus càng mạnh.
Tóm lại: bệnh viêm gan B tình trạng nhiễm HBv hiện tại có thể được xác định dựa trên sự dương tính của bất kỳ chỉ số nào sau đây:
① HBsAg huyết thanh dương tính; HBV DNA hoặc DNA polymerase huyết thanh dương tính;
③ kháng thể kháng HBc huyết thanh IgM dương tính;
④ HBcAG trong gan và (hoặc ) HBsAg dương tính hoặc HBVDNA dương tính. Có những thay đổi bất thường trên siêu âm gan và điện tâm đồ.
Xem thêm:
Dịch sốt xuất huyết, cách phân biệt và điều trị