Phương trình căn bản của Vinylaxetilen
29 Tháng Chín, 2021Vinylaxetilen là nguyên liệu chính để tạo ra cao su tổng hợp. Cùng tò mò về công thức vinylaxetilen, phản ứng của vinylaxetilen...
Clo – Cl
Contents
Clo là halogen nhẹ thứ hai và được biểu diễn dưới dạng Cl. Số hiệu nguyên tử của nguyên tố hóa học này là 17.
Nó xuất hiện dưới dạng khí màu vàng xanh nhạt. Clo lỏng có thể gây bỏng da và clo ở dạng khí gây kích ứng màng nhầy. Vị trí của nó theo bảng tuần hoàn là giữa flo và brom. Cấu hình điện tử của nó là [Ne] 3s 2 3p 5 . Có hai đồng vị của clo là bền.
Chúng là 37 Cl và 35 Cl. 36 Cl là đồng vị phóng xạ bền của clo. Natri clorua là hợp chất phổ biến nhất của clo trong khi hợp chất đơn giản nhất là hydro clorua. Natri clorua có công thức phân tử NaCl trong khi hiđro clorua có công thức phân tử HCl. Nó có tính phản ứng cao. Carl Wilhelm Scheele , một nhà hóa học người Thụy Điển đã phát hiện ra Clo vào năm 1774.
| Cl | Clo |
| Số nguyên tử | 17 |
| Trọng lượng nguyên tử | 35,453 |
| Độ nóng chảy | −101,5 ° C |
| Điểm sôi | −34,04 ° C |
Clo là halogen thứ hai trong bảng tuần hoàn, là một phi kim ở nhóm 17. Do đó, các tính chất của nó tương tự như flo, brom và iot, và nói chung là trung gian trong số hai tính chất đầu tiên. Clo có cấu hình electron [Ne] 3s23p5, với bảy electron đóng vai trò là electron hóa trị của nó ở lớp thứ ba và lớp ngoài cùng. Như tất cả các halogen, do đó, nó thiếu một electron so với một octet đầy đủ, và do đó là một chất oxy hóa mạnh, tương tác với các nguyên tố khác để hoàn thành lớp vỏ bên ngoài của nó.
Nguyên tố này là trung gian về độ âm điện giữa flo và brom (độ âm điện của flo là 3,98, độ âm điện của clo là: 3,16, độ âm điện của brom là 2,96 và độ âm điện của iot là 2,66). Nguyên tố này phản ứng kém hơn flo và phản ứng mạnh hơn brom, phù hợp với các mẫu tuần hoàn. Mặc dù nó là chất oxi hóa yếu hơn flo nhưng lại mạnh hơn brom. Để so sánh, ion clorua là một chất khử yếu hơn bromua, nhưng mạnh hơn florua.
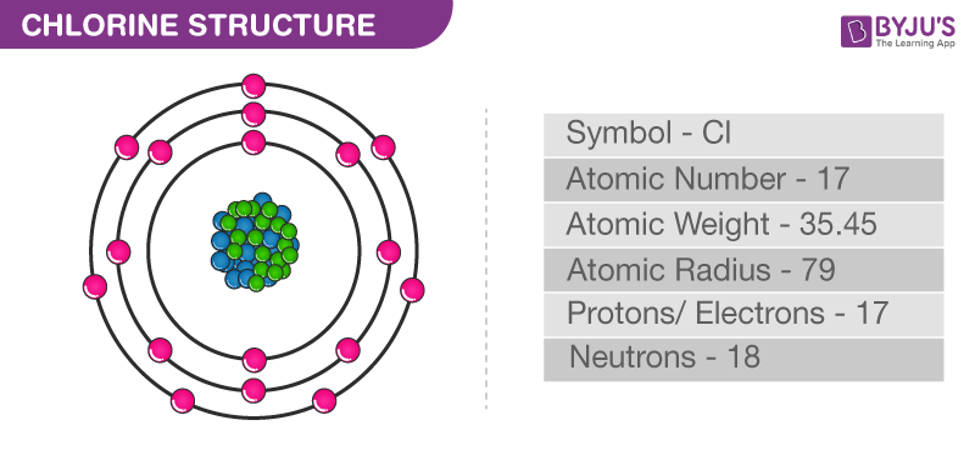

Cấu trúc clo
Số hiệu nguyên tử của clo là 17. Điều này có nghĩa rằng clo chứa tổng số 17 proton và 17 electron trong cấu trúc nguyên tử của nó. Các electron này được sắp xếp thành 3 lớp vỏ electron sơ cấp. Lớp electron thứ nhất của clo chứa tổng cộng hai electron trong khi lớp electron thứ hai của clo chứa 8 electron. Cuối cùng, lớp vỏ electron ngoài cùng của nguyên tử clo (thường được gọi là lớp vỏ hóa trị) chứa tổng cộng 7 electron. Do đó, hóa trị của clo thường được coi là 7. Tuy nhiên, điều quan trọng cần lưu ý là clo chỉ cần thêm một electron để hoàn thành cấu hình octet của nó. Do đó, hóa trị của clo cũng có thể được coi là 1.
Clo là một bảng tuần hoàn ở nhóm 17, còn được gọi là halogen, và không được tìm thấy trong tự nhiên như một nguyên tố chỉ như một hợp chất. Muối, hoặc natri clorua, và các hợp chất kali sylvite là phổ biến nhất.
Clo không ổn định là kết quả của sự tiếp xúc thứ cấp khá khó xảy ra từ những người tiếp xúc, nhưng khí clo có thể ngưng tụ trên da và gây ô nhiễm cho những người khác khi tiếp xúc qua da.
Clo chứa 17 electron. Điều này có nghĩa là có 17 proton trong mỗi nguyên tử này. 17 electron. Nơtron 35-17 = 18.
Ở nhiệt độ thường, clo là chất khí màu vàng lục. Clo có mùi hăng, khó chịu, giống như chất tẩy trắng, có thể được phát hiện ở mức độ thấp. Nồng độ khí clo lớn hơn không khí khoảng 2,5 lần, điều này ban đầu sẽ khiến nó ở gần mặt đất ở những nơi có không khí chuyển động thấp.
Clo dạng khí rất độc và được xếp vào danh sách những chất gây kích ứng phổi. Nó có khả năng hòa tan trong nước trung bình với khả năng gây tổn thương cấp tính đường hô hấp trên và dưới. Do có mùi nồng nên có thể dễ dàng phát hiện ra khí clo.
Xem thêm: