Công thức Strontium Nitrate là gì ? Cùng tìm hiểu về nó.
21 Tháng Mười Hai, 2021Contents Công thức Strontium Nitrate Công thức nitrat stronti, còn được gọi là công thức Stronti dinitrat hoặc công...
Contents
Công thức bari bromua, còn được gọi là công thức Bari (2+) dibromit hoặc công thức Bariumbromit được thảo luận trong bài viết này. Nó hoạt động như một muối đơn giản ở dạng nước trong khi nó kết tinh trong mô-típ clorua chì tạo thành các tinh thể trắng hình thoi mê sảng. Công thức phân tử hoặc công thức hóa học của Bari bromua là BaBr 2 (khan).
Bari (2+) đibromua có thể được tổng hợp từ bari cacbonat hoặc bari sulfua bằng cách phản ứng với axit hydrobromic (HBr) để tạo thành bari bromua ngậm nước.
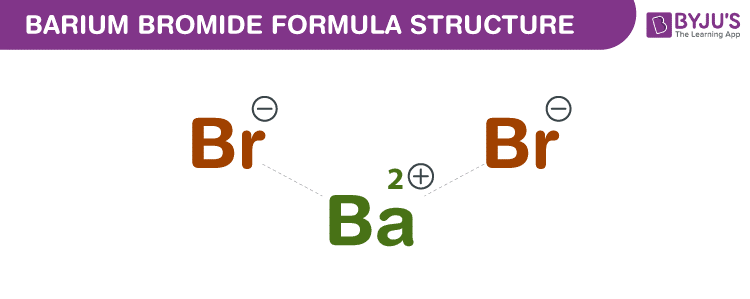

| Công thức hóa học của Bari bromua | BaBr 2 (khan) |
| Khối lượng phân tử của Bari bromua | 297,14 g / mol (khan) |
| Mật độ của Bari bromua | 4,78 g / cm 3 (khan) |
| Điểm sôi của Bari bromua | 1,835 ° C |
| Điểm nóng chảy của Bari bromua | 857 ° C |
Bari bromua và một số muối bari hòa tan trong nước khác được coi là độc hại vì chúng có thể gây ngộ độc nghiêm trọng khi ăn phải.
Xem thêm:
| Chứng chỉ IELTS là gì? Có tác dụng gì? | Chứng chỉ Toeic là gì? Có tác dụng gì? |
| Chứng chỉ tin học là gì? Quy định của cơ quan nào? | Chứng chỉ năng lực xây dựng là gì? Cơ quan nào cấp? |