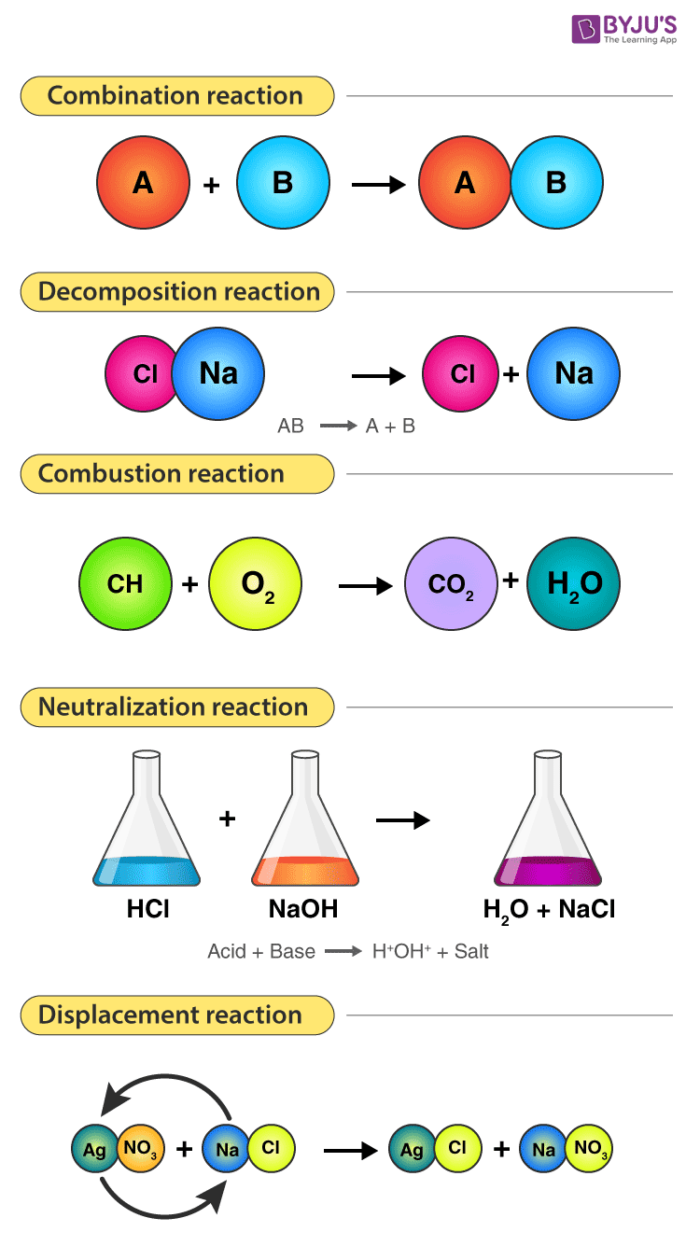

Các loại phản ứng hóa học khác nhau – Phản ứng kết hợp, phân hủy, cháy, trung hòa và chuyển vị
Trong một phản ứng hóa học, các chất phản ứng được gọi là chất phản ứng trong khi các chất được tạo thành trong một phản ứng hóa học được gọi là sản phẩm . Dưới đây sẽ thảo luận sáu loại phản ứng hóa học phổ biến .
| Các loại phản ứng hóa học | Giải trình | Phản ứng chung |
| Phản ứng kết hợp | Hai hoặc nhiều hợp chất kết hợp với nhau để tạo thành một hợp chất. | A + B → AB |
| Phản ứng phân hủy | Ngược lại với phản ứng kết hợp – một phân tử phức tạp bị phá vỡ để tạo ra những phân tử đơn giản hơn. | AB → A + B |
| Phản ứng kết tủa | Hai dung dịch gồm các muối tan được trộn lẫn với nhau, tạo thành chất rắn (kết tủa) không tan. | A + Muối tan B → Kết tủa + muối tan C |
| Phản ứng trung hòa | Một axit và một bazơ phản ứng với nhau. Nói chung, sản phẩm của phản ứng này là muối và nước. | Axit + Bazơ → Muối + Nước |
| Phản ứng đốt cháy | Oxy kết hợp với một hợp chất để tạo thành carbon dioxide và nước. Các phản ứng này tỏa nhiệt, nghĩa là chúng tỏa nhiệt. | A + O 2 → H 2 O + CO 2 |
| Phản ứng chuyển vị | Một phần tử diễn ra với một phần tử khác trong hợp chất. | A + BC → AC + B |
Contents
Các loại phản ứng hóa học khác nhau
5 loại phản ứng hóa học chính là:
- Phản ứng kết hợp
- Phản ứng phân hủy
- Phản ứng chuyển vị
- Phản ứng dịch chuyển kép
- Phản ứng kết tủa
1. Phản ứng kết hợp
- Một phản ứng trong đó hai hoặc nhiều chất phản ứng kết hợp với nhau để tạo thành một sản phẩm duy nhất được gọi là phản ứng kết hợp.
- Nó có dạng X + Y → XY
- Phản ứng kết hợp còn được gọi là phản ứng tổng hợp.
- Ví dụ về phản ứng kết hợp: 2Na + Cl 2 → 2NaCl
2. Phản ứng phân hủy
- Phản ứng trong đó một hợp chất đơn lẻ phân hủy thành hai hoặc nhiều hợp chất đơn giản hơn được gọi là phản ứng phân hủy.
- Nó có dạng XY → X + Y
- Phản ứng phân hủy chỉ ngược lại với phản ứng kết hợp.
- Ví dụ về phản ứng phân hủy: CaCO 3 → CaO + CO 2
- Phản ứng trong đó một hợp chất bị phân hủy do đun nóng được gọi là phản ứng phân hủy nhiệt.
3. Phản ứng chuyển vị
- Một phản ứng hóa học trong đó một nguyên tố phản ứng mạnh hơn thay thế một nguyên tố kém phản ứng hơn khỏi dung dịch muối nước của nó.
- Nó có dạng X + YZ → XZ + Y
- Nó còn được gọi là phản ứng thay thế
- Ví dụ về phản ứng chuyển vị: Zn + CuSO 4 → ZnSO 4 + Cu
4. Phản ứng chuyển vị kép
- Một phản ứng hóa học trong đó các ion được trao đổi giữa hai chất phản ứng tạo thành một hợp chất mới được gọi là phản ứng chuyển vị kép.
- Nó có dạng XY + ZA → XZ + YA
- Nó còn được gọi là phản ứng metathesis
- Ví dụ về phản ứng chuyển vị kép:
BaCl 2 + Na 2 SO 4 → BaSO 4 + 2NaCl
5. Phản ứng kết tủa
- Một phản ứng hóa học bao gồm sự tạo thành một sản phẩm không hòa tan (kết tủa; chất rắn) được gọi là phản ứng kết tủa.
- Các chất phản ứng có thể hòa tan, nhưng sản phẩm tạo thành sẽ không hòa tan và tách ra ở dạng rắn.
- Phương trình hóa học trong đó sự thay đổi hóa học được mô tả là thích hợp cho phản ứng trong dung dịch, nhưng đối với phản ứng của các hợp chất ion trong dung dịch nước (nước), phương trình phân tử điển hình có các cách biểu diễn khác nhau.
- Một phương trình phân tử có thể chỉ ra công thức của chất phản ứng và sản phẩm không có mặt và loại bỏ hoàn toàn công thức của các ion là chất phản ứng và sản phẩm thực.
- Nếu chất trong phương trình phân tử thực sự tồn tại dưới dạng ion phân ly được viết dưới dạng ion của chúng, thì kết quả là một phương trình ion.
Phản ứng kết tủa xảy ra khi một dung dịch, ban đầu chứa các chất hòa tan, tạo ra chất rắn, thường đặc hơn và rơi xuống đáy bình phản ứng.
Các phản ứng kết tủa phổ biến nhất xảy ra trong dung dịch nước liên quan đến việc hình thành một hợp chất ion không hòa tan khi hai dung dịch chứa các hợp chất hòa tan được trộn lẫn với nhau. Hãy nhận xét hiện tượng xảy ra khi cho dung dịch nước NaCl vào dung dịch nước AgNO 3 . Dung dịch đầu tiên chứa các ion Na + và Cl – ngậm nước và dung dịch thứ hai chứa các ion Ag + và NO 3 – .
NaCl (s) → Na + (aq) + Cl – (aq)
AgNO 3 (s) → Ag + (aq) + NO 3 – (aq)
Khi trộn lẫn sẽ xảy ra phản ứng chuyển đôi, tạo thành hợp chất tan NaNO 3 và hợp chất không tan AgCl. Trong bình phản ứng, các ion Ag + và Cl – kết hợp với nhau, và tạo ra chất rắn màu trắng trong dung dịch. Khi chất rắn kết tủa, các ion Na + và NO 3 – vẫn còn trong dung dịch.
Phản ứng chuyển đôi tổng thể được biểu diễn bằng phương trình cân bằng sau:
NaCl (aq) + AgNO 3 (aq) → AgCl (s) + NaNO 3 (aq)
Vấn đề ví dụ
- Khi trộn dung dịch nước gồm Pb (NO 3 ) 2 và KI thì có tạo thành kết tủa không?
- Viết một phương trình cân bằng cho phản ứng tạo kết tủa xảy ra khi dung dịch nước của đồng (II) iotua và kali hiđroxit được kết hợp.
Dung dịch:
Bạn được yêu cầu dự đoán liệu kết tủa sẽ hình thành trong một phản ứng hóa học và viết một phương trình cân bằng cho phản ứng tạo kết tủa.
Bạn được cung cấp danh tính của hai chất phản ứng.
1. Đúng, một kết tủa rắn, PbI 2 , tạo thành khi trộn các dung dịch này:
Pb (NO 3 ) 2 (aq) + KI (aq) → PbI 2 (s) + 2KNO 3 (aq)
2. Hai sản phẩm của phản ứng là đồng (II) hiđroxit và kali iotua tan .
CuI 2 (aq) + 2 KOH (aq) → Cu (OH) 2 (s) + 2 KI (aq)
Câu hỏi thường gặp – Câu hỏi thường gặp
Làm thế nào để bạn xác định một phản ứng hóa học?
Một phản ứng hóa học thường được theo sau bởi các dấu hiệu vật lý có thể dễ dàng phát hiện, chẳng hạn như sự tỏa nhiệt và ánh sáng, sự hình thành kết tủa, sự biến đổi khí hoặc sự thay đổi bề ngoài.
Làm thế nào để bạn xác định các thay đổi vật lý và hóa học?
Hình dạng hoặc hình thức của vật chất thay đổi thông qua quá trình chuyển đổi vật chất, nhưng loại vật chất trong vật chất thì không. Tuy nhiên, trong một sự thay đổi hóa học, loại vật chất thay đổi và ít nhất một vật chất mới với các đặc tính mới được tạo ra. Không có vết cắt thẳng của khoảng cách giữa chuyển đổi vật lý và hóa học.
Tại sao chúng ta viết một phương trình hóa học?
Mục đích của việc viết một phương trình hóa học cân bằng là để giải thích các chất phản ứng xảy ra (nguyên liệu ban đầu) và sản phẩm (kết quả cuối cùng). Tỷ lệ mà họ trả lời để bạn có thể đo lường lượng chất phản ứng bạn cần và số lượng hàng hóa bạn có thể sản xuất.
Phản ứng hóa học và phương trình là gì?
Phương trình hóa học là sự biểu diễn ký hiệu dưới dạng các ký hiệu và công thức của một phản ứng hóa học, trong đó các thực thể phản ứng ở phía bên trái và các thực thể sản phẩm ở phía bên phải được đưa ra.
Phương trình bộ xương là gì?
Một phương trình khung là khi mỗi sản phẩm tham gia phản ứng được viết với các công thức hóa học mô tả phản ứng hóa học. Ví dụ: Phương trình số hạng: oxy + metan. Đioxit với cacbon + Hơi.
Xem thêm: