Trong phần này, chúng ta sẽ nghiên cứu các phần tử của khối P và các tính chất của chúng.
Chủ đề liên quan
Phần tử khối P bao gồm
- Nhóm 13 Nguyên tố: Họ Boron
- Nhóm 14 Nguyên tố: Họ cacbon
- Nhóm 15 Nguyên tố: Họ nitơ
- Nhóm 16 Nguyên tố: Họ oxy
- Nhóm 17 Nguyên tố: Họ flo
- Nhóm 18 Nguyên tố: Họ Neon
Bạn có biết vị trí của các phần tử khối P trong Bảng tuần hoàn không?
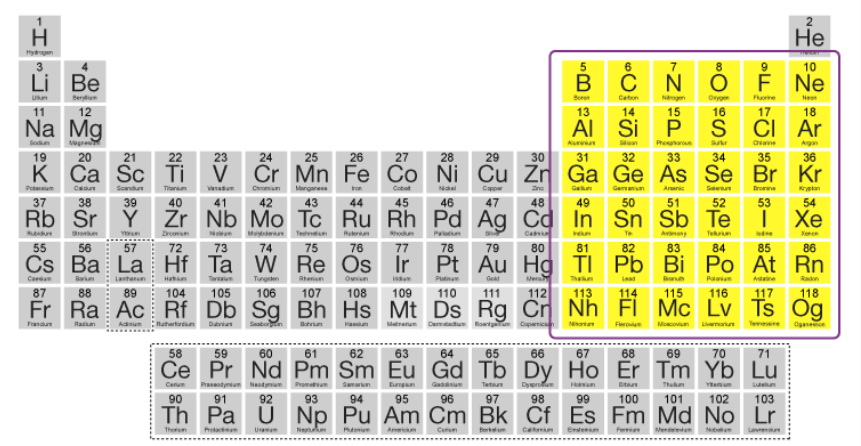

Các nguyên tố khối P không là gì khác ngoài nguyên tố mà electron cuối cùng đi vào lớp vỏ p ngoài cùng. P khối bắt đầu từ 13 tháng nhóm và đi đến 18 ngày nhóm trong bảng tuần hoàn.
Bạn chắc hẳn đã thấy rằng than được sử dụng trong các làng để nấu thức ăn. Nó không là gì khác ngoài một nguyên tố khối P tức là cacbon. Kim cương được sử dụng để làm đồ trang trí đẹp cũng được tạo thành từ carbon. Lá nhôm được tạo thành từ nhôm cũng được tạo thành từ phần tử khối p.
Đặc điểm của phần tử khối p
- Các cấu hình điện tử chung của các nguyên tố p-block là ns 2 np 1-6 (trừ Anh) . Trong khi cấu hình điện tử lõi bên trong có thể khác nhau. Chỉ vì sự khác biệt này trong lõi bên trong mà có những thay đổi cả về tính chất vật lý và hóa học của các nguyên tố.
- Trạng thái oxi hoá của các nguyên tố trong khối p là cực đại khi nó bằng tổng số electron hoá trị tức là tổng số electron của S và P. Một trong những điều thú vị nhất về các nguyên tố khối p là nó chứa cả phi kim loại và kim loại.
Thành viên đầu tiên của các phần tử khối p khác với các phần tử khác ở hai khía cạnh chính:
- Đầu tiên là kích thước và mỗi và mọi tài sản phụ thuộc vào kích thước.
- Sự khác biệt thứ hai chỉ áp dụng cho nguyên tố khối p, phát sinh từ ảnh hưởng của các obitan d trong vỏ hóa trị của các nguyên tố nặng hơn.
Các câu hỏi thường gặp
Phần tử khối P là gì?
Khối p là khu vực của bảng tuần hoàn bao gồm cột IIIA đến cột VIIIA và không bao gồm heli. Có 35 nguyên tố khối p, tất cả đều ở obitan p với các electron hóa trị. Các phần tử khối p là một nhóm các phần tử rất đa dạng với nhiều thuộc tính.
Tại sao chúng được gọi là phần tử khối P?
Các nguyên tố khối s và khối p được gọi như vậy bởi vì các điện tử hóa trị của chúng nằm trong một quỹ đạo s hoặc p. Chúng thường được gọi là các Thành phần Chuẩn, để phân biệt chúng với chuỗi biến đổi và biến đổi bên trong.
17 phi kim loại là gì?
Các phi kim loại nằm ở cực bên phải của bảng tuần hoàn, ngoại trừ hydro, được tìm thấy ở góc trên bên trái. 17 nguyên tố phi kim loại là: Hydro, Heli, Carbon, Nitrogen, Oxy, Flo, Neon, Photpho, Lưu huỳnh, Clo, Argon, Selen, Brom, Krypton, Iod, Xenon và Radon.
Những tính chất của phi kim loại là gì?
Thông thường phi kim loại giòn khi ở thể rắn và thường có tính dẫn nhiệt và dẫn điện thấp. Về mặt hóa học, các phi kim loại có xu hướng có năng lượng tương đối cao từ quá trình ion hóa, tiếp xúc với các electron và độ âm điện. Khi chúng phản ứng với các nguyên tố và hợp chất hóa học khác, chúng nhận hoặc trao đổi các electron.
Cấu hình điện tử chung của các phần tử khối P là gì?
Cấu hình bên ngoài điện tử chung cho các thành phần khối p là ns 2 np (1−6) . (n − 1) d (1−10) ns (0−2) là cấu hình điện tử chung bên ngoài của các thành phần khối d. Cấu hình điện tử chung của phần tử khối F ngoài cùng là (n − 2) f (0−14) (n − 1) d (0−1) ns 2 .
Xem thêm: