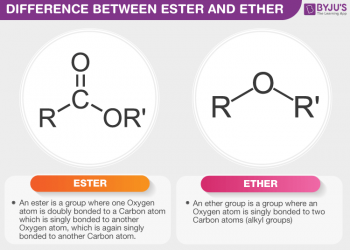
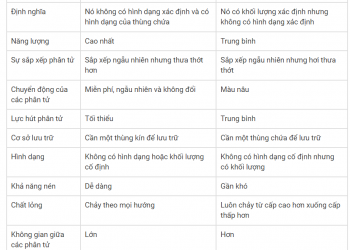
Một nucleophile thường được tích điện âm hoặc trung tính với một vài electron duy nhất có thể cưỡng lại được. H 2 O, -OMe hoặc -OtBu là một số ví dụ. Nhìn chung, chất giàu điện tử là một chất nucleophile . Các electron thường mang điện tích dương hoặc là các hạt trung tính với các obitan trống bị hút vào một trung tâm giàu electron.
Các phản ứng hóa học xảy ra giữa người cho và người nhận electron được mô tả bằng các khái niệm như electrophin và nucleophile . Đây là những khái niệm quan trọng nhất trong hóa học hữu cơ. Chúng đã thay thế các thuật ngữ cationoid và anionoid và được giới thiệu vào năm 1933.
Contents
Electrophile là gì?
Các loài mang điện tích cực hoặc trung tính được gọi là các electrophin thiếu electron và có thể nhận một vài electron. Chúng còn được gọi là những loài ưa electron (philic).
- Thuật ngữ electrophile có thể được chia thành “điện” bắt nguồn từ điện tử và “phile” có nghĩa là yêu thương.
- Chúng bị thiếu điện tử và do đó yêu cầu điện tử.
- Chúng được tích điện dương hoặc tích điện trung tính.
- Chúng hút các electron. Chuyển động của các electron phụ thuộc vào mật độ.
- Chúng chuyển từ khu vực có mật độ cao sang khu vực có mật độ thấp.
- Chúng trải qua các phản ứng cộng electrophin và phản ứng thế thế electrophin .
- Electrophile còn được gọi là axit Lewis.
Nucleophile là gì?
Nucleophile là thuốc thử bao gồm một nguyên tử cặp electron vô song hoặc đơn lẻ. Vì một nucleophile giàu điện tử, nó sẽ tìm kiếm các vị trí thiếu điện tử, tức là hạt nhân có nghĩa là hạt nhân yêu thương. Nucleophile hoạt động như bazơ Lewis, theo ý niệm của Lewis về axit và bazơ.
- Thuật ngữ nucleophile có thể được chia thành “nucleo” có nguồn gốc từ hạt nhân và “phile” có nghĩa là yêu thương.
- Chúng giàu electron và do đó hạt nhân có tính yêu thương. Chúng mang điện tích âm hoặc tích điện trung tính.
- Họ tặng các electron.
- Chuyển động của các electron phụ thuộc vào mật độ.
- Chúng di chuyển từ khu vực có mật độ thấp sang khu vực có mật độ cao.
- Chúng trải qua các phản ứng bổ sung nucleophilic và thay thế nucleophilic.
- Một nucleophile còn được gọi là bazơ Lewis.
Ví dụ, vì nitơ có độ âm điện nhỏ hơn oxy, amoniac là chất nucleophile mạnh hơn nước. Điều này có nghĩa là cặp amoniac đơn độc liên kết nitơ lỏng lẻo hơn so với cặp nước đơn độc liên kết oxy.
Để bạn hiểu rõ electrophin và nucleophile khác nhau như thế nào , dưới đây là một số điểm khác biệt chính giữa nguyên tử và ion:
Sự khác biệt giữa Electrophile và Nucleophile
| Sự khác biệt giữa Electrophile và Nucleophile được liệt kê dưới đây. | |
|---|---|
| ĐIỆN TỬ | NUCLEOPHILE |
| Còn được gọi là axit Lewis | Còn được gọi là cơ sở Lewis |
| Chúng được tích điện dương / trung tính | Chúng được tích điện âm / trung tính |
| Chúng trải qua các phản ứng cộng electrophin và phản ứng thế thế electrophin | Chúng trải qua các phản ứng bổ sung nucleophilic và thay thế nucleophilic |
| Thiếu điện tử | Giàu điện tử |
| Nó nhận một cặp electron để tạo thành liên kết cộng hóa trị | Nó cho một cặp electron để tạo thành liên kết cộng hóa trị |
| Tất cả cacbocation | Tất cả các carbanion |
| Ví dụ: Ion Hydronium | Ví dụ: Ion clorua |
Đây là một số khác biệt quan trọng giữa nucleophile và electrophile . Một phối tử có thể bị tấn công ngay lập tức bởi một nucleophile hoặc một electrophin khi được kích hoạt khi ở gần kim loại. Mỗi cuộc tấn công này có thể dẫn đến phản hồi cho một phép bổ sung hoặc phần trừu tượng.
Xem thêm:
Kiến thức mới nhất về Vectơ kết quả