Tầm quan trọng của nước (H2O) đọc dễ hiểu
18 Tháng Mười Một, 2021Contents Nước là gì? Nước là một chất hóa học không màu và trong suốt, là thành phần chính...
Contents
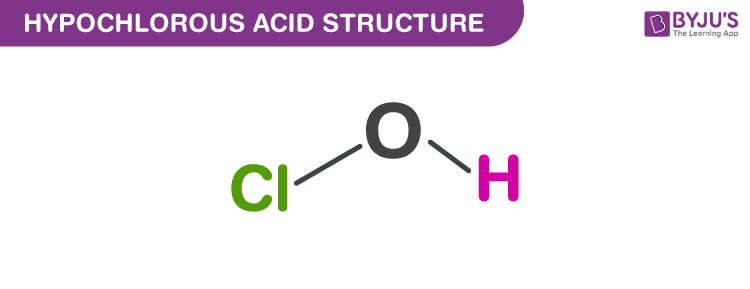
HOCl là một axit yếu với tên hóa học Hypochlorous Acid. Nó còn được gọi là Hydro hypochlorite hoặc Clo hydroxit hoặc axit hypochloric. Nó được phát hiện bởi một nhà hóa học người Pháp Antoine Jerome Balard vào năm 1834. Nó là một oxyacid của clo.
Nó chứa clo đơn trị có chức năng như một tác nhân khử hoặc một tác nhân oxy hóa. Nó là một axit không ổn định và hoạt động như một chất chuyển hóa của con người. Nó thuộc họ các loài oxy phản ứng và là một axit liên hợp của hypochlorite.
| HOCl | Axit hypoclorơ |
| Trọng lượng phân tử của HOCl | 52,457 g/mol |
| Không. của người chấp nhận liên kết hydro | 1 |
| Khối đơn vị của axit hypoclorơ | 51,972 g/mol |
| Không. của nhà tài trợ liên kết hydro | 1 |

HClO ⇌ ClO− + H+
Hypochlorites là muối của axit hypoclorơ. Một trong những hypochlorites phổ biến là natri hypochlorite (NaClO), là một thành phần hoạt chất trong thuốc tẩy.
2 HClo(aq) + 2 H + 2 e+− ⇌ Cl2 (g) + 2 H2O
Trong đó, E = +1,63 V
HClO + HCl → H2O + Cl2
Nh3 + HClO → NH2Cl + H2O
Axit hypoclorơ thường được sử dụng làm chất khử trùng trong dung dịch rửa vệ sinh và bể bơi. Đối với các ứng dụng như vậy, clo được áp dụng cho nước để hòa tan các hóa chất phản ứng trong dung dịch.
Bằng cách thêm axit vào muối nước của axit hypoclorơ (chẳng hạn như natri hypochlorite trong dung dịch thuốc tẩy thương mại), phản ứng kết quả được đẩy sang trái và khí clo được tạo ra. Do đó, hòa tan khí clo vào các dung dịch nước đơn giản, chẳng hạn như natri hydroxit, thúc đẩy việc tạo ra các chất tẩy trắng hypochlorite rắn.
Axit hypoclorơ phản ứng dễ dàng với các axit amin sở hữu các chuỗi bên của nhóm amin, với clo HClO thay thế hydro dẫn đến chloramine hữu cơ. Axit amin clo hóa phân hủy nhanh chóng, nhưng protein clorat tồn tại lâu hơn và giữ lại một số khả năng oxy hóa.
Xem thêm:
Thụ phấn là gì? Quá trình thụ phấn và Các loại thụ phấn
Hoa đào trong tiếng anh được định nghĩa và phát âm như thế nào ?
Công cụ tìm căn bậc hai là gì? Xem xong 5 phút hiểu luôn.