Tính chất và công dụng của Amoni Hydroxit (Nh4OH) chi tiết nhất
12 Tháng Bảy, 2021Contents NH4OH là gì ? NH4OH là công thức hóa học của dung dịch amoniac trong nước. Dung dịch...
Contents
Lưu huỳnh điôxít có thành phần hóa học của SO2 và cũng thường được gọi là anhydride axit lưu huỳnh, anhydride lưu huỳnh hoặc oxit lưu huỳnh.
Hợp chất này là một phân tử uốn cong và có thứ tự liên kết là 1,5. Cấu trúc cộng hưởng có thể được mô tả bằng lý thuyết liên kết hóa trị bằng cách sử dụng quỹ đạo s và p.
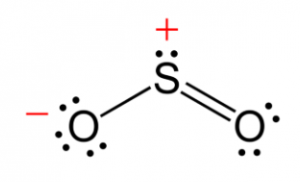

Cấu trúc của Sulphur Dioxide
1. Trong phòng thí nghiệm, sulphur dioxide được điều chế bằng phản ứng của sunfat kim loại hoặc bisulphite kim loại với axit loãng. Ví dụ, một phản ứng giữa axit sulphuric loãng và natri sunfat sẽ dẫn đến sự hình thành SO2.
Na2như vậy3 + H2như vậy4 → Na2như vậy4 + H2O + SO2
2. Về mặt thương mại, nó thu được dưới dạng một sản phẩm bổ trợ được giải phóng từ việc rang các loại ores sunfua. Khí thu được được sấy khô, hóa lỏng và sau đó được lưu trữ trong xi lanh thép.
4FeS2 (s) + 11 O2 (g) →2Fe2O3 (s) + 8SO2 (g)


H2O + SO2 → H2như vậy3
2H2S + SO2 → 3S + 2H2O
như vậy2 + 2H2O → H2như vậy4 + 2H
Các biện pháp an toàn phải được thực hiện chống lại lưu huỳnh điôxít vì hít phải loại khí này gây ra các vấn đề sức khỏe nghiêm trọng như tử vong sớm và các vấn đề về hô hấp.
câu hỏi
Điều gì xảy ra khi
H đậm đặc2như vậy4 được thêm vào canxi florua
SO3 được truyền qua nước?
giải pháp
Nó tạo thành hydro florua
Caf2 + H2như vậy4 –> CaSO4 + 2HF
Nó hòa tan trong nước cho H2như vậy4
như vậy3 + H2O –> H2như vậy4
Lưu huỳnh điôxít, (SO2), chất vô cơ, một loại khí độc hại, dày, không màu. Trong các bước trung gian sản xuất axit sulfuric, nó được sản xuất với số lượng lớn. Lưu huỳnh điôxít có mùi hăng, khó chịu tương tự như mùi hương của một trận đấu vừa bị đánh.
Lưu huỳnh điôxít, SO2, là một loại khí hoặc chất lỏng không màu có mùi mạnh, có mùi. Nó có nguồn gốc từ việc đốt nhiên liệu hóa thạch (than và dầu) và nấu chảy quặng khoáng sản chứa lưu huỳnh (nhôm, đồng, kẽm, chì và sắt). Lưu huỳnh điôxít nhanh chóng hòa tan để tạo thành axit sulfuric trong nước.
Lưu huỳnh điôxít là một loại khí axit, và điều này có thể dễ dàng chứng minh bằng cách thêm nước và một vài giọt chỉ số phổ quát vào một thùng chứa khí. Axit kết quả là axit sulphurous (H2SO3) là axit dibasic yếu.
Mưa axit xảy ra khi được giải phóng vào khí quyển bởi lưu huỳnh điôxít (SO2) và oxit nitơ (NOX) và được mang theo dòng gió và không khí. So2 và NOX phản ứng để tạo thành axit sulfuric và nitric với nước, oxy và các hóa chất khác. Sau đó, chúng kết hợp trước khi thả xuống bàn, với nước và các vật liệu khác.
Trong các loại nước ép có độ axit cao ít lưu huỳnh dioxide là cần thiết, ví dụ 15 mg l−1 với lưu huỳnh dioxide miễn phí ở pH 3.0 có tác dụng kháng khuẩn tương tự như 150 mg l−1 ở pH 4,0 Tỷ lệ sulfite, bisulfit và lưu huỳnh phân tử dioxide trong dung dịch nước như một chức năng của pH.
Xem thêm:
Lợi nhuận là gì? Xem xong 5 phút hiểu luôn.
Các Vấn Đề Về Diện Tích Và Chu Vi Của Một Vòng Tròn là gì? Xem xong 5 phút hiểu luôn.
Lãi và lỗ theo tỷ lệ phần trăm là gì? Xem xong 5 phút hiểu luôn.