Tính chất và công dụng của Natri sunfat (Na2SO3) chi tiết nhất
13 Tháng Bảy, 2021Contents Natri sunfat là gì? Natri sunfat (Na2SO3) là một chất rắn màu trắng, hòa tan trong nước, kết...
Contents
Axit axetic là một hợp chất hữu cơ có công thức CH3COOH. Nó là một axit cacboxylic bao gồm một nhóm methyl được gắn vào một nhóm chức carboxyl. Tên IUPAC có hệ thống của axit axetic là axit ethanoic và công thức hóa học của nó cũng có thể được viết là C2H4O2. Giấm là dung dịch axit axetic trong nước và chứa từ 5% đến 20% axit ethanoic theo thể tích. Mùi hăng và vị chua là đặc trưng của axit axetic có trong đó.
Một dung dịch axit axetic không pha loãng thường được gọi là axit axetic băng. Nó tạo thành các tinh thể xuất hiện như băng ở nhiệt độ dưới 16,6OC. Nó có một loạt các ứng dụng như một dung môi cực, protic. Trong lĩnh vực hóa học phân tích, axit axetic băng được sử dụng rộng rãi để ước tính các chất có tính kiềm yếu.
Cấu trúc của axit axetic được minh họa dưới đây.
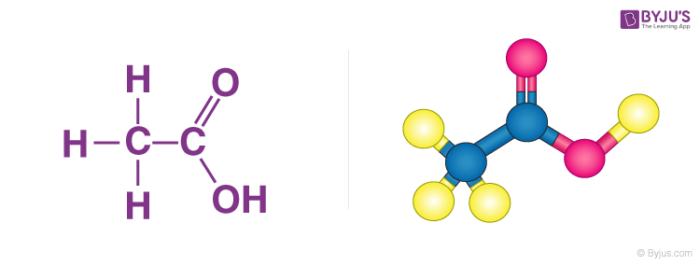

Về mặt cấu trúc, axit ethanoic là axit cacboxylic đơn giản thứ hai (đơn giản nhất là axit formic, HCOOH), và về cơ bản là một nhóm methyl có nhóm chức carboxyl gắn liền với nó.
Axit axetic được sản xuất công nghiệp thông qua quá trình cacbonyl hóa methanol. Các phương trình hóa học cho ba bước liên quan đến quá trình này được cung cấp dưới đây.
Ở đây, một chất trung gian methyl iodide được tạo ra từ phản ứng giữa methanol và hydro iodide. Chất trung gian này sau đó được phản ứng với carbon monoxide và hợp chất kết quả được xử lý bằng nước để đủ khả năng cho sản phẩm axit axetic. Điều quan trọng cần lưu ý là một phức hợp carbonyl kim loại phải được sử dụng làm chất xúc tác cho bước 2 của quá trình này.
Một số muối naphthalene của coban, crom và mangan có thể được sử dụng làm chất xúc tác kim loại trong quá trình oxy hóa acetaldehyde. Phương trình hóa học cho phản ứng này có thể được viết là:
O2 + 2CH3CHO → 2CH3COOH
Ethylene (C)2H4) có thể bị oxy hóa thành axit axetic với sự trợ giúp của chất xúc tác paladi và axit dị hợp tử, như được mô tả bởi phản ứng hóa học sau đây.
O2 + C2H4 → CH3COOH
Một số vi khuẩn kỵ khí có khả năng chuyển đổi trực tiếp đường thành axit axetic.
C6H12O6 → 2CH3COOH
Có thể lưu ý rằng không có chất trung gian ethanol nào được hình thành trong quá trình lên men kỵ khí của đường bởi những vi khuẩn này.
Mặc dù axit ethanoic được coi là một axit yếu, ở dạng đậm đặc, nó sở hữu sức mạnh ăn mòn mạnh mẽ và thậm chí có thể tấn công da người nếu tiếp xúc với nó. Một số tính chất chung của axit axetic được liệt kê dưới đây.
Sự trao đổi chất của carbohydrate và chất béo ở nhiều động vật tập trung xung quanh sự liên kết của axit axetic với coenzyme A. Nói chung, hợp chất này được sản xuất thông qua phản ứng giữa methanol và carbon monoxide (cacbonyl hóa methanol).
Các phản ứng hóa học được trải qua bởi axit axetic tương tự như các axit cacboxylic khác. Khi đun nóng đến nhiệt độ trên 440OC, hợp chất này trải qua quá trình phân hủy để tạo ra metan và carbon dioxide hoặc nước và ethenone, như được mô tả bởi các phương trình hóa học sau đây.
Ch3COOH + Co → nhiệt2 + CH4
Ch3COOH + Nhiệt → H2C=C=O + H2O
Một số kim loại như magiê, kẽm và sắt trải qua sự ăn mòn khi tiếp xúc với axit axetic. Những phản ứng này dẫn đến sự hình thành muối axetat.
2CH3COOH + Mg → Mg (CH)3COO)2 (magiê axetat) + H2
Phản ứng giữa axit ethanoic và magiê dẫn đến sự hình thành magiê axetat và khí hydro, như được mô tả bởi phương trình hóa học được cung cấp ở trên.
Axit axetic phản ứng với kiềm và tạo thành muối axetat, như được mô tả dưới đây.
Ch3COOH + KOH → CH3ĐẦU BẾP + H2O
Hợp chất này cũng tạo thành muối axetat bằng cách phản ứng với cacbonat (cùng với carbon dioxide và nước). Ví dụ về các phản ứng như vậy bao gồm:
2CH3COOH + Na2Đồng3 (natri cacbonat) → 2CH3COONa + CO2 + H2O
Ch3COOH + NaHCO3 (natri bicarbonate) → CH3COONa + CO2 + H2O
Phản ứng giữa PCl5 và axit ethanoic dẫn đến sự hình thành ethanoyl clorua.
Axit ethanoic là một hợp chất hữu cơ rất quan trọng trong cuộc sống hàng ngày của con người. Một số công dụng quan trọng của axit axetic được liệt kê dưới đây.
Ở trạng thái lỏng, CH3COOH là một hydrophile (dễ dàng hòa tan trong nước) và cũng là một dung môi cực, protic. Một hỗn hợp axit axetic và nước, theo cách này, tương tự như hỗn hợp ethanol và nước. Axit axetic cũng tạo thành hỗn hợp miscible với hexane, chloroform và một số loại dầu. Tuy nhiên, nó không tạo thành hỗn hợp khó cưỡng với các ankan chuỗi dài (chẳng hạn như octan).
Các tính chất dung môi mong muốn của axit axetic, cùng với khả năng hình thành hỗn hợp không thể trộn với cả các hợp chất cực và không phân cực, làm cho nó trở thành một dung môi công nghiệp rất quan trọng. Nó được sử dụng rộng rãi trong chế phẩm công nghiệp của dimethyl terephthalate (DMT).
Ứng dụng phổ biến nhất của axit axetic là việc sử dụng nó trong giấm. Nó cũng cực kỳ hữu ích trong việc sản xuất monome vinyl acetate (thường được viết tắt là VAM). Monome này là một điều kiện tiên quyết quan trọng trong sản xuất sơn và chất kết dính.
Không, CH3COOH là một axit yếu. Nó chỉ trải qua sự phân ly hoàn toàn khi nó được phản ứng với một cơ sở mạnh mẽ. Axit clohydric là một axit mạnh hơn nhiều so với axit axetic.
Nó có thể được điều chế bằng cách phản ứng methanol với hydro iodide và thêm carbon monoxide vào sản phẩm (methyl iodide) để có được acetyl iodide. Khi thủy phân, acetyl iodide tạo ra axit axetic.
Xem thêm: